Control de calidad en instalaciones radiológicas
Introducción
El control de calidad en instalaciones radiológicas tiene como objetivo garantizar la obtención de imágenes diagnósticas de alta calidad, minimizando la exposición a radiaciones tanto para pacientes como para el personal. Este proceso incluye acciones planificadas y sistemáticas que aseguran el correcto funcionamiento de los equipos y procedimientos, contribuyendo a la precisión en los diagnósticos médicos.
Conceptos básicos
- Calidad: Conjunto de especificaciones y características de un servicio o producto que permiten satisfacer las necesidades conocidas o previstas de los usuarios.
- Programa de Garantía de Calidad (GC): Esfuerzo organizado del personal de un servicio para asegurar que las imágenes diagnósticas producidas sean de calidad suficiente, con el menor coste y la mínima exposición a radiaciones.
- Control de calidad: Parte de la garantía de calidad que incluye actividades como vigilancia, evaluación y mantenimiento de las características operativas de los equipos.
Componentes de la garantía de calidad
1. Personas:
- Pacientes: El proceso comienza desde su ingreso al servicio hasta la obtención del diagnóstico, asegurando un trato adecuado.
- Personal técnico: Los técnicos de radiología y radiólogos trabajan en equipo para garantizar la eficacia y eficiencia del servicio.
- Personal administrativo y auxiliar: Proporcionan apoyo logístico y organizativo.
2. Instalaciones y equipos:
- El mantenimiento adecuado y el control de calidad de los equipos son esenciales para obtener imágenes precisas que permitan a los médicos especialistas realizar diagnósticos confiables.
3. Resultados:
- Imágenes diagnósticas de alta calidad y diagnósticos precisos que coincidan con la evaluación clínica del paciente.
Métodos operativos en los programas de garantía de calidad
Los principales métodos utilizados incluyen:
– Protocolos de exploraciones: Comparar los procedimientos empleados localmente con las recomendaciones internacionales para optimizar las técnicas utilizadas.
– Análisis de exploraciones repetidas: Identificar causas de repeticiones totales o parciales de estudios para reducir errores.
– Análisis de placas desechadas: Evaluar las causas de rechazo de imágenes para implementar mejoras.
– Dosimetría personal y de área: Monitorear la exposición a la radiación del personal y el entorno.
– Análisis de dosis a pacientes: Realizar mediciones periódicas para optimizar la exposición y garantizar la seguridad.
– Relación entre exploraciones y pacientes atendidos: Evaluar la eficiencia del servicio mediante el análisis del número y tipo de exploraciones realizadas.
Componentes clave del control de calidad
1. Pruebas de aceptación: Garantizan que los equipos cumplen con los requisitos iniciales antes de ser utilizados.
2. Evaluación del funcionamiento habitual: Asegura que los equipos operan correctamente durante su uso diario.
3. Mantenimiento y corrección de errores: Minimiza interrupciones y asegura un funcionamiento continuo y seguro.
Calidad en radiodiagnóstico
La calidad en este ámbito implica optimizar la obtención de imágenes diagnósticas y proteger a los pacientes y trabajadores de exposiciones innecesarias a la radiación. Los equipos deben mantenerse en condiciones óptimas, y los protocolos deben ajustarse para minimizar riesgos y maximizar resultados.
Requisitos normativos
Aunque se mencionan normativas específicas, en términos generales, las unidades asistenciales de radiodiagnóstico deben:
- Asegurar la obtención de imágenes optimizadas.
- Proteger a los pacientes y al personal de la exposición innecesaria a la radiación.
- Garantizar que las dosis recibidas sean tan bajas como razonablemente sea posible.
Este enfoque integral asegura la seguridad y eficiencia del servicio, contribuyendo al bienestar del paciente y al cumplimiento de estándares internacionales.
Programa de garantía de calidad en radiodiagnóstico
Implementación obligatoria
Todas las unidades de radiodiagnóstico deben contar con un programa de garantía de calidad desde el inicio de su funcionamiento. Este programa debe seguir protocolos actualizados, ya sean nacionales o internacionales, y tiene como objetivo garantizar la seguridad, eficacia y optimización de los procedimientos radiológicos.
Contenido mínimo del programa
1. Justificación y optimización de las exploraciones radiológicas: Se debe asegurar que cada exploración esté debidamente justificada y se realice con técnicas optimizadas para minimizar la exposición a la radiación.
2. Control de calidad:
– Equipos radiológicos.
– Sistemas de registro y procesado de imágenes.
– Equipos de visualización (monitores, negatoscopios).
– Instrumentos de medición.
3. Evaluación de dosis:
– Análisis periódico de las dosis administradas a los pacientes en las exploraciones más comunes.
– Comparación de los valores obtenidos con los valores de referencia establecidos.
– Establecimiento de medidas correctivas si los valores superan los límites recomendados.
4. Revisión de imágenes rechazadas o repetidas: Se analizarán las razones para identificar y reducir errores.
5. Recursos humanos y materiales:
– Descripción detallada de los recursos necesarios.
– Definición de responsabilidades y niveles de autoridad del personal.
6. Formación:
– Capacitación para el uso de equipos radiológicos.
– Entrenamiento continuo en protección radiológica y en técnicas clínicas.
7. Verificación anual:
– Evaluación de los niveles de radiación en las áreas de trabajo y accesibles al público.
8. Gestión de incidentes:
– Registro de eventos relacionados con incidentes o accidentes durante las exploraciones.
– Investigación de las causas y aplicación de medidas correctoras.
Procedimientos en exploraciones con rayos X
El programa debe incluir protocolos escritos para cada tipo de práctica radiológica estándar, actualizados regularmente y diseñados para minimizar la dosis absorbida por los pacientes, garantizando la obtención de información diagnóstica adecuada.
- Pacientes especiales: En casos como niños, mujeres embarazadas o técnicas que impliquen altas dosis, se deberán tomar medidas adicionales para reducir riesgos.
- Responsabilidad médica: El médico especialista supervisará la justificación del uso de rayos X y la elección de las técnicas más apropiadas.
Procedimientos intervencionistas
Los procedimientos que implican el uso de rayos X deben realizarse en salas diseñadas específicamente para este propósito, con equipos adecuados y operados por médicos especializados y debidamente cualificados.
Control de calidad clínico
El programa debe establecer:
- La necesidad y justificación de las pruebas diagnósticas.
- La responsabilidad del médico en la supervisión y realización de las exploraciones.
- La selección de técnicas radiológicas apropiadas para minimizar las dosis sin comprometer la calidad diagnóstica.
- La elaboración de informes diagnósticos claros.
Control de calidad del equipamiento
- Pruebas esenciales: Los equipos serán sometidos a controles de calidad basados en protocolos reconocidos, nacionales o internacionales.
- Coordinación: Un responsable designado en el programa garantizará la evaluación del equipamiento, emitiendo informes sobre su estado y las medidas correctoras aplicadas.
- Detección de anomalías:
- Si se detectan problemas que comprometan la seguridad o la calidad de las imágenes, se realizarán pruebas adicionales para identificar las causas.
- En casos graves, se suspenderá temporalmente el uso del equipo hasta su reparación.
Este enfoque asegura la seguridad del paciente, la calidad de las imágenes y el cumplimiento de los estándares internacionales en radiodiagnóstico.
Archivo de la documentación
El titular del centro sanitario donde funcione una unidad asistencial de radiodiagnóstico está obligado a conservar los informes generados por la actividad de la unidad durante períodos establecidos:
1. Informes clínicos y técnicos:
– Los informes relacionados con procedimientos y actividades, como los mencionados en protocolos internos, deben conservarse por un período de 30 años.
2. Informes de equipos:
– Aquellos relacionados con el estado y funcionamiento de los equipos radiológicos se archivarán durante toda la vida útil del equipo.
3. Acceso a la documentación:
– Estos archivos estarán disponibles para las autoridades sanitarias competentes y el Consejo de Seguridad Nuclear, que podrán requerirlos en cualquier momento.
4. En caso de cierre del centro:
– Si el centro sanitario cesa sus operaciones, el titular está obligado a enviar la documentación a las autoridades sanitarias y al Consejo de Seguridad Nuclear, según corresponda a sus competencias.
Indicadores básicos de calidad
Los indicadores básicos incluyen la verificación de la dosis de radiación administrada a los pacientes y los niveles de radiación en áreas de trabajo y espacios accesibles al público.
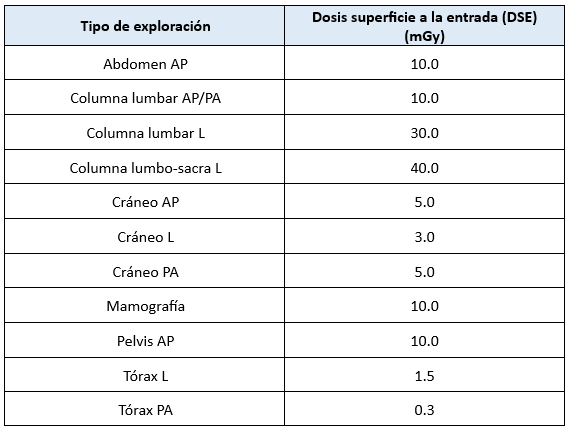
Verificación de dosis en pacientes
1. Exploraciones estándar:
– Las dosis y la calidad de imagen se controlarán en exploraciones habituales, como cráneo, tórax, columna lumbar, pelvis, abdomen y mama.
– Para radiología dental intraoral, se establece un valor de referencia de 7 mGy como dosis superficial en radiografías periapicales.
2. Pacientes pediátricos:
– Los valores de referencia serán menores que los utilizados para adultos, considerando la mayor sensibilidad a la radiación.
3. Prohibición de irradiación innecesaria:
– No se realizará irradiación de pacientes con el único fin de controlar la calidad de los equipos.
4. Registro y evaluación:
– Los resultados de las mediciones se documentarán en informes específicos.
Verificación de niveles de radiación en áreas de trabajo y públicas
1. Medición en puestos de trabajo y áreas públicas:
- Los niveles de radiación deben medirse regularmente en las áreas donde trabajan los profesionales y en espacios accesibles al público.
2. Instrumentos de medición:
- Se pueden utilizar:
– Cámaras de ionización con capacidad para medir energía de fotones desde 25 keV y con una precisión del ±15%.
– Dosímetros de termoluminiscencia.
– Otros sistemas aprobados que cumplan los requisitos técnicos necesarios.
3. Documentación:
- Los resultados de estas mediciones se registrarán en informes oficiales, garantizando la trazabilidad de los datos.
Este sistema de archivo y verificación asegura la transparencia, el cumplimiento normativo y la protección de los pacientes, el personal y el público.
Criterios para la aceptabilidad de instalaciones de radiodiagnóstico
Este anexo establece los parámetros y criterios aplicables para evaluar la calidad y seguridad de los equipos utilizados en radiología convencional.
1. Parámetros técnicos de los equipos
A) Tensión del tubo
- Calibración de la escala: La diferencia máxima permitida entre el valor nominal y el real no debe superar el 10%.
- Variación con cambios en la corriente del tubo: No debe exceder el 10%.
- Reproducibilidad: En mediciones repetidas, la variación no debe superar el 5% del valor promedio.
B) Filtración total
- El haz útil debe tener una filtración equivalente superior a 2,5 mm de Al para tensiones mayores a 70 kVp.
C) Tiempo de exposición
- Para exposiciones nominales mayores a 100 ms, la variación del tiempo real respecto al indicado debe ser inferior al 10%.
D) Rendimiento del tubo
- Valor mínimo: Debe ser mayor a 25 μGy/mAs a 1 metro, con una tensión de 80 kVp y una filtración mayor a 2,5 mm de Al.
- Reproducibilidad: La variación no debe exceder el 20% en exposiciones repetidas bajo condiciones similares.
- Cambios de corriente (mA): La variación debe ser inferior al 15%.
- Cambios en la carga (mAs): La variación debe ser inferior al 10%.
2. Alineación y colimación
A) Coincidencia del haz de rayos X con el haz luminoso
- La diferencia entre los bordes respectivos del campo luminoso y el de rayos X no debe superar el 3% de la distancia foco-receptor.
B) Alineación del haz de rayos X con el receptor de imagen
- El centro del haz de rayos X y el del receptor no deben diferir más del 2% de la distancia foco-receptor.
C) Colimación
- El área expuesta debe mantenerse dentro de los bordes del receptor de imagen, con un margen de desviación máximo del 2% en cualquier lado.
D) Colimación automática
- Debe ser posible reducir el campo de exposición a áreas más pequeñas que el receptor de imagen seleccionado.
3. Calidad de la imagen
A) Rejilla y artefactos
- Las imágenes obtenidas no deben presentar artefactos ni evidencias visibles de las láminas de la rejilla móvil.
B) Control automático de exposición (CAE)
- Variación con el tiempo de exposición: La diferencia en densidad óptica (DO) entre exposiciones cortas y largas no debe superar ± 0,3 DO.
- Variación con la tensión del tubo: La diferencia en densidad óptica entre exposiciones realizadas con diferentes tensiones no debe superar ± 0,3 DO.
- Variación con el espesor del atenuador: Para tensiones fijas, las diferencias en densidad óptica no deben exceder ± 0,3 DO.
4. Radiación de fuga
- La radiación de fuga desde la carcasa del equipo, medida a 1 metro del foco, no debe exceder 1 mGy/h bajo las condiciones máximas especificadas por el fabricante.
Estos criterios están diseñados para garantizar que los equipos de radiología convencional funcionen de manera segura, precisa y eficiente, respetando los estándares de calidad y minimizando riesgos tanto para pacientes como para operadores.
Control de calidad en el revelado de placas, propiedades de los receptores de imagen y condiciones de visualización
A) Pantallas intensificadoras y chasis
1. Estado y limpieza:
- No deben presentarse artefactos visibles en las placas expuestas y reveladas.
2. Hermeticidad del chasis:
- Se debe probar la hermeticidad exponiendo un chasis con película no expuesta durante 10 minutos bajo una luz intensa (mínimo 1,000 cd/m²). Al revelar, no deben aparecer bordes negros en la película.
3. Contacto pantalla-película:
- El chasis no debe generar zonas de densidad desigual o imágenes borrosas. Esto puede verificarse utilizando una malla metálica colocada sobre el chasis.
4. Sensibilidad relativa:
- Las combinaciones pantalla-película deben ofrecer resultados homogéneos en términos de densidad óptica bajo condiciones similares.
B) Revelado de placas
1. Base y velo:
- La combinación de base y velo no debe superar los 0,30 DO.
2. Índice de velocidad:
- Las desviaciones respecto al valor inicial deben ser inferiores a 0,20 DO.
3. Índice de contraste:
- La variación respecto al valor inicial o de referencia debe ser inferior a 0,20 DO.
C) Cuarto oscuro
1. Entradas de luz:
- Con las luces apagadas y adaptando la vista durante al menos 5 minutos, no debe detectarse luz infiltrada.
2. Luces de revelado:
- Al exponer una película previamente irradiada con una densidad óptica cercana a 1,0 DO, la densidad adicional provocada por las luces de revelado no debe exceder 0,10 DO.
D) Condiciones de visualización
1. Negatoscopio:
- El brillo mínimo debe ser de 1,700 cd/m².
- La uniformidad en el brillo no debe variar más del 30%.
2. Luz ambiental:
- A un metro del negatoscopio, la iluminación ambiental no debe superar los 50 lux.
Control de calidad en fluoroscopia
1. Tasa de dosis máxima
- En fluoroscopia convencional, la tasa máxima en la entrada de la pantalla sin rejilla debe ser inferior a 0,8 μGy/s con un maniquí adecuado (20 cm de polimetilmetacrilato, PMMA).
- En procedimientos que requieran altas dosis, esta tasa no debe exceder 1,0 μGy/s.
2. Resolución de contraste y espacial
- Para combinaciones de intensificador de imagen y sistema de televisión, la resolución mínima debe ser:
- 0,8 pares de líneas/mm para campos de 30-35 cm.
- 1,4 pares de líneas/mm para campos más pequeños (15-25 cm).
3. Sensibilidad a bajo contraste
- La sensibilidad en funcionamiento automático, estimada desde el monitor, debe ser 4% o inferior.
4. Advertencias de tiempo
- Los equipos deben incluir un dispositivo que avise al operador tras un tiempo máximo predefinido, que no debe exceder los 10 minutos.
Cinefluorografía convencional
1. Tasa de dosis:
- La tasa de dosis en la entrada del intensificador no debe superar 0,20 μGy/s para un intensificador de imagen de 23 cm.
2. Tasas de dosis típicas:
- Las dosis habituales en pacientes oscilan entre 0,10 y 0,30 Gy/min con un maniquí de 20 cm de PMMA.
3. Campo de radiación:
- La relación entre el campo de radiación y la entrada del intensificador de imagen no debe ser mayor a 1,15.
Estos criterios garantizan la calidad del proceso de revelado, la integridad de los receptores de imagen y las condiciones óptimas de visualización y fluoroscopia.
Requisitos para tomografía convencional y computarizada, radiografía dental y mamografía
1. Tomografía convencional
- Altura del corte: La diferencia entre la altura indicada y la medida debe ser menor de ±5 mm.
- Incremento del plano de corte: Al pasar de un plano a otro, la altura del corte debe ser reproducible con una variación inferior a ±2 mm.
- Uniformidad de la altura del corte: La imagen de un objeto estándar, como una lámina de plomo, debe ser uniforme, sin solapamientos inesperados ni variaciones anómalas.
- Resolución espacial: El equipo debe ser capaz de resolver al menos 1,6 pares de líneas/mm (pl/mm).
2. Tomografía computarizada (TC)
- Ruido de la imagen: La desviación estándar de los números de TC en una región homogénea no debe superar el 20% del valor de referencia.
- Valores de TC: La desviación de los números de TC en diferentes materiales no debe exceder ±20 UH o el 5% del valor teórico.
- Índice de dosis de tomografía computarizada (IDTC): Los valores deben mantenerse dentro de una variación del ±20% respecto al valor de referencia.
- Espesor de corte: La anchura medida a la mitad de la altura máxima del perfil de dosis no debe variar más del ±20% respecto al valor de referencia.
- Resolución espacial y de bajo contraste: Detalles de 0,35 cm deben ser visibles en un maniquí estándar de agua con valores coherentes según el diseño del equipo.
3. Radiografía dental
- Calidad del haz:
– La tensión mínima del tubo debe ser de 50 kV.
– La filtración del haz debe ser de 1,5 mm de Al para tensiones de hasta 70 kV y de 2,5 mm de Al para tensiones superiores.
- Distancia foco-piel:
– Mínimo 20 cm para tensiones superiores a 60 kV.
– Mínimo 10 cm para tensiones de hasta 60 kV.
- Diámetro del campo:
– Máximo de 60 mm en el extremo del haz de radiación.
- Reproducibilidad y rendimiento:
– Variación de tiempos de exposición inferior al 10%.
– Rendimiento del tubo de 30-80 μGy/mAs a 1 m para tensiones de 50-70 kV.
4. Mamografía
Generación y control del haz:
- Dosis: La tasa de dosis a una distancia igual a la foco-película debe ser superior a 7,5 mGy/s.
- Alineación del haz:
- Los rayos deben cubrir completamente la película sin exceder los bordes en más de 5 mm.
Control automático de exposición (CAE):
- Densidad óptica:
- El valor debe mantenerse dentro de ±0,15 DO del valor previsto.
- La densidad óptica por escalón en el selector de densidad debe estar entre 0,10 y 0,20 DO.
- Reproducibilidad:
- En tiempos cortos, la desviación no debe exceder el 5%.
- En tiempos largos, la variación debe ser menor de ±0,20 DO respecto al valor de referencia.
- Compensación por espesor y tensión:
- Las variaciones de densidad deben estar dentro de ±0,15 DO respecto al valor de referencia.
Compresión:
- Fuerza de compresión: La fuerza debe ser firme pero tolerable, entre 130 y 200 N (13 a 20 kg).
- Alineación de la placa de compresión:
- La desalineación máxima permitida es de 15 mm para cargas asimétricas y 5 mm para cargas simétricas.
Rejilla antidifusora y procesamiento:
- Factores de exposición: El intervalo de exposiciones no debe superar el ±5%.
- Procesado de la película:
- Base y velo menor de 0,2 DO.
- Índice de velocidad dentro del ±10% respecto al valor de referencia.
Condiciones de visualización:
- Negatoscopio: Brillo entre 2,000 y 6,000 cd/m² y luz ambiental inferior a 50 lux.
- Kerma en aire: Para maniquíes de diferentes espesores, el valor máximo permitido es:
- <10 mGy para 40 mm de PMMA.
- <12 mGy para 45 mm de PMMA.
- <20 mGy para 50 mm de PMMA.
Resolución espacial y sensibilidad al contraste:
- Resolución espacial: Mínimo de 12 pares de líneas/mm en condiciones específicas.
- Contraste de bajo nivel: En detalles grandes, el contraste debe ser inferior al 1,3% para maniquíes de 45 mm de PMMA.
- Tiempo de exposición: Debe ser menor de 2 segundos para maniquíes de 45 mm.
Estos estándares aseguran la seguridad, precisión y calidad de los equipos de tomografía, radiografía dental y mamografía, promoviendo diagnósticos efectivos y confiables.
Control de calidad de equipos convencionales de radiografía
El control de calidad en los equipos de radiografía convencional es esencial para garantizar la seguridad del paciente y la precisión en las imágenes diagnósticas. A continuación, se detallan los parámetros principales que deben ser evaluados:
1. Parámetros geométricos
- Colimación:
- El haz útil de rayos X debe coincidir con el campo luminoso del colimador. Las desviaciones no deben superar el 2% de la distancia fuente-receptor de imagen.
- Desajustes en colimación pueden generar irradiación innecesaria y mayor dispersión, afectando la calidad de la imagen y aumentando la exposición.
2. Calidad del haz
- Filtración:
- El haz útil debe estar filtrado adecuadamente para eliminar radiaciones de baja energía que no aportan información diagnóstica y solo incrementan la dosis al paciente.
- Kerma en aire:
- La energía en la superficie de entrada debe ser inferior a:
- 10 mGy para 40 mm de PMMA.
- 12 mGy para 45 mm de PMMA.
- 20 mGy para 50 mm de PMMA.
- La energía en la superficie de entrada debe ser inferior a:
3. Tiempo de exposición
- Reproducibilidad:
- Para exposiciones cortas, la desviación del promedio debe ser menor al 5%.
- Para exposiciones largas, la variación debe ser inferior a ±0,20 DO respecto a la densidad óptica de referencia.
4. Rendimiento
- Variación con espesor del objeto:
- Las diferencias en densidad óptica al cambiar el espesor deben mantenerse dentro de ±0,15 DO respecto al valor de referencia.
- Variación con la tensión del tubo:
- Las variaciones en densidad óptica debido a cambios en la tensión del tubo deben estar dentro de ±0,15 DO.
5. Rejilla antidifusora y receptor de imagen
- Factores de exposición:
- El rango de exposición en diferentes chasis debe estar dentro de un margen del ±5%.
- Densidad óptica:
- La diferencia máxima entre chasis no debe superar los 0,20 DO.
6. Procesado de la película
- Base y velo:
- Para películas convencionales, este valor debe ser inferior a 0,20 DO.
- Índice de velocidad:
- Variación dentro del ±10% respecto al valor de referencia.
- Contraste:
- El gradiente medio debe ser al menos 2,8.
7. Condiciones de visualización
- Negatoscopio:
- El brillo debe estar entre 2,000 y 6,000 cd/cm².
- La iluminación ambiental en el área de trabajo no debe superar los 50 lux.
8. Calidad de la imagen
- Resolución espacial:
- Con una rejilla de resolución a 4 cm por encima del receptor, la resolución debe ser superior a 11 pl/mm en las dos direcciones principales del foco.
- Sensibilidad a bajo contraste:
- Para un maniquí de 45 mm de PMMA, el umbral de contraste debe ser inferior al 1,3% para detalles de 6 mm.
- Tiempo de exposición:
- El tiempo necesario para obtener la imagen en un maniquí de 45 mm de PMMA debe ser inferior a 2 segundos.
Estos parámetros garantizan que los equipos funcionen correctamente, minimizando la exposición innecesaria y mejorando la precisión diagnóstica.
Control de calidad en equipos convencionales de radiografía
El control de calidad en equipos de radiografía convencional es fundamental para garantizar la precisión de los diagnósticos y la seguridad del paciente. Este proceso se enfoca en verificar aspectos geométricos, la calidad del haz de radiación, los tiempos de exposición y el rendimiento del equipo. A continuación, se describen los principales puntos a evaluar:
1. Parámetros geométricos
- Colimación:
- El área del haz de rayos X debe coincidir con el campo luminoso del colimador.
- Desajustes en colimación pueden provocar irradiación innecesaria y afectar la calidad de la imagen. La desviación máxima permitida es del 2% respecto a la distancia fuente-receptor.
- Tamaño del punto focal:
- Afecta la resolución espacial de las imágenes.
- Se mide utilizando herramientas como:
- Estenoscopio: Preciso, pero requiere más tiempo.
- Patrón en estrella: Más rápido, pero limitado en tamaños menores a 0,3 mm.
- Cámara de hendidura: Método más común y efectivo.
2. Calidad del haz
- Filtración:
- Se utiliza para eliminar las radiaciones de baja energía que no contribuyen a la imagen y solo aumentan la dosis al paciente.
- La filtración mínima equivalente debe ser de 2,5 mm de aluminio, de los cuales 1,5 mm deben ser permanentes.
- Para evaluar la filtración se emplea la capa hemirreductora (CHR), que mide la atenuación del haz.
- Resolución espacial:
- Se mide en pares de líneas por milímetro (pl/mm), evaluando la capacidad del sistema para distinguir detalles finos.
3. Tiempo de exposición
- Reproducibilidad:
- Las variaciones en tiempos cortos no deben superar el 5% del valor medio.
- En tiempos largos, el margen permitido es de ±20%.
- Calibración:
- Se realiza anualmente para asegurar que los tiempos seleccionados en el panel de control correspondan a los aplicados durante la exposición.
- Métodos como el plato giratorio o el osciloscopio se utilizan para equipos de diferentes fases y frecuencias.
4. Rendimiento
- Consistencia:
- La cantidad de radiación producida debe ser constante, con una variación menor al 10%.
- Medición:
- Se utiliza un dosímetro de precisión para verificar que los valores de mA y ms estén dentro de los límites establecidos.
5. Control de exposición
- Sistemas automáticos:
- Algunos equipos poseen sistemas automáticos que ajustan los parámetros de exposición, como los fotocronómetros, los cuales requieren calibración regular.
- Densidad óptica:
- Los ajustes deben asegurar que las imágenes obtenidas tengan una densidad uniforme y dentro de los valores de referencia.
6. Procedimientos generales
- Calibración del kilovoltaje:
- Se realiza para garantizar que los valores seleccionados en el panel correspondan a los utilizados en el haz.
- Métodos de calibración incluyen:
- Cámaras de ionización.
- Fotodiodos.
- Osciloscopios (los más precisos).
- Verificación anual:
- La revisión general del equipo debe realizarse al menos una vez al año, salvo en casos de detección de fallos.
Beneficios del control de calidad
- Seguridad del paciente:
- Minimización de la exposición a radiaciones innecesarias.
- Calidad de la imagen:
- Obtención de imágenes claras y precisas para diagnósticos confiables.
- Durabilidad del equipo:
- Identificación y corrección de problemas antes de que afecten el rendimiento.
Otros elementos a considerar en el control de calidad en radiología
El control de calidad incluye también la evaluación y mantenimiento de diversos elementos relacionados con el funcionamiento y seguridad del equipo de radiología. Estos elementos son esenciales para garantizar la calidad de las imágenes y la protección del paciente y el personal.
1. Pantallas intensificadoras
- Mantenimiento y limpieza:
- Es necesario limpiar las pantallas intensificadoras regularmente para evitar artefactos en las imágenes.
- La frecuencia de limpieza depende de la carga de trabajo en la sala de radiodiagnóstico, pero se recomienda al menos una vez al mes.
- Verificación anual:
- Se debe comprobar el contacto entre la pantalla y la película mediante:
- Radiografías de un patrón de malla metálica.
- Análisis de zonas borrosas que puedan indicar fallos.
- Se debe comprobar el contacto entre la pantalla y la película mediante:
2. Sistemas de protección
- Material de protección radiológica:
- Incluye delantales de plomo, protectores gonadales y tiroideos, y guantes plomados.
- Se debe evaluar su estado mediante exposiciones controladas a radiación ionizante, observando si presentan deterioro o pérdida de efectividad.
- Blindajes estructurales:
- Es necesario verificar que los elementos de protección, como paredes plomadas, mantengan su capacidad de absorción de radiaciones.
3. Negatoscopios
- Mantenimiento de la iluminación:
- La intensidad luminosa de los negatoscopios debe ser uniforme y no variar más del 1% entre diferentes áreas.
- Si se detectan diferencias significativas, deben reemplazarse las bombillas o componentes defectuosos.
4. Reproducibilidad de la exposición
- Cada disparo del equipo debe reproducir los parámetros seleccionados para obtener imágenes uniformes en las mismas condiciones.
- Se utiliza un dosímetro de precisión para verificar la consistencia de la intensidad de radiación.
- Este control debe realizarse al menos una vez al año, con un margen de variación inferior al 8%.
Control de calidad en fluoroscopia
1. Condiciones seriográficas
- Exposición correcta:
- Depende del kilovoltaje, miliamperaje y la sensibilidad de la combinación película-pantalla.
- Reducción de dosis:
- La fluoroscopia moderna utiliza técnicas como la fotofluorografía, que disminuyen la exposición del paciente y requieren menos personal y material.
2. Tasas de exposición
- Control de la dosis cutánea de entrada:
- No debe superar los 50 mGy/min.
- Se evalúa con un dosímetro de precisión que verifica la tasa de exposición en condiciones normales.
3. Sistemas de exposición automática
- Control automático de brillo:
- Estos sistemas estabilizan el brillo de la imagen independientemente del grosor o densidad de la zona anatómica explorada.
- Requieren controles periódicos porque su uso continuado puede llevar a deterioro o errores en la exposición.
- Prueba con fantoma:
- Se utiliza un fantoma de prueba para verificar que el brillo sea constante bajo condiciones predefinidas.
- Los valores recomendados se encuentran entre 10-40 μR/s, dependiendo del sistema.
Beneficios del control regular
- Mejora de la calidad de las imágenes diagnósticas.
- Protección del paciente al reducir la exposición innecesaria.
- Garantía de un funcionamiento óptimo de los equipos y sistemas asociados.
Control de calidad en tomografía computarizada (TC)
La calidad de imagen en tomografía computarizada (TC) es esencial para obtener diagnósticos precisos. Este proceso implica la evaluación de parámetros clave que aseguren la claridad, contraste y resolución necesarios para identificar estructuras anatómicas normales o patológicas.
1. Parámetros de calidad en TC
A) Resolución de densidades (contraste)
- Definición:
- Relación entre las zonas más claras y oscuras de la imagen. Un contraste adecuado permite distinguir detalles en tejidos de diferente densidad.
- Tipos de contraste:
- Alto contraste:
- Presente en tejidos densos como el hueso.
- Bajo contraste:
- Aparece en tejidos con alto contenido acuoso, como músculos, vísceras y vasos sanguíneos. En estos casos, el sistema mejora la resolución mediante algoritmos de procesamiento.
- Alto contraste:
- Importancia:
- Se busca maximizar el contraste para detectar lesiones pequeñas y sutiles.
B) Resolución espacial
- Definición:
- Capacidad del equipo para representar con precisión los contornos de objetos con alto contraste.
- Medición:
- A través de funciones específicas como:
- Función de respuesta del borde (FRB).
- Función de transferencia de modulación (FTM).
- Dispositivo de alineación (izquierda-derecha).
- A través de funciones específicas como:
- Comparación:
- Similar a la radiología convencional, pero los sistemas TC permiten mediciones objetivas mediante números calculados matemáticamente.
C) Ruido
- Definición:
- Señal no deseada que genera un efecto granulado en la imagen.
- Medición:
- Como la desviación estándar porcentual de los valores de píxeles en un barrido realizado sobre un baño de agua.
- Factores que afectan al ruido:
- Voltaje incorrecto.
- Filtración inadecuada del haz.
- Miliamperaje inapropiado (dosis insuficiente o excesiva).
- Grosor del corte (colimadores mal ajustados).
- Eficiencia de los detectores.
- Tamaño del píxel y la ventana de visualización.
2. Uso de fantomas en el control de calidad
- Función del fantoma:
- Simula el cuerpo humano, reproduciendo las condiciones reales de radiación y dispersión.
- Permite colocar sondas detectoras en puntos específicos para medir diferentes dosis.
- Dosis evaluadas:
- Dosis superficial.
- Dosis media.
- Dosis profundas y laterales (izquierda-derecha).
- Dosis única (media aritmética de las mediciones).
- Resultados:
- Los datos se muestran en el visor digital del medidor, permitiendo ajustar los parámetros del equipo.
3. Consideraciones adicionales
- Protocolización:
- Es imprescindible definir parámetros de exploración estandarizados para cada tipo de estudio.
- Supervisión periódica:
- El control regular del equipo garantiza la estabilidad de los parámetros y previene errores en las imágenes obtenidas.
El control de calidad en TC asegura imágenes confiables, reduce dosis innecesarias y optimiza la detección de patologías. Este proceso contribuye directamente a la seguridad del paciente y la eficacia del diagnóstico.
Control de calidad en tomografía computarizada (TC)
El control de calidad en los equipos de tomografía computarizada es crucial para garantizar la precisión en los diagnósticos, reducir errores y optimizar las imágenes. A continuación, se detallan aspectos fundamentales del control de calidad, la linealidad del sistema y las correcciones necesarias para artefactos.
1. Linealidad
- Definición:
- Es la capacidad del escáner para calibrar los números TC en función de la densidad del agua (valor 0) y otros materiales, asegurando que los coeficientes de atenuación sean correctos.
- Procedimiento de calibración:
- Se realiza diariamente utilizando dispositivos como el Catphan, diseñado para medir diferentes parámetros de calidad, como:
- Exactitud de los números TC en materiales (aire, agua, LDPE, entre otros).
- Uniformidad del campo exploratorio.
- Nivel de ruido.
- Resolución espacial en alto contraste.
- Se realiza diariamente utilizando dispositivos como el Catphan, diseñado para medir diferentes parámetros de calidad, como:
2. Artefactos en TC
Los artefactos son imágenes falsas que no corresponden a la realidad y pueden llevar a interpretaciones erróneas. Se dividen en dos categorías principales:
A) Artefactos de origen físico
- Endurecimiento del haz:
- Ocurre cuando el haz de rayos X atraviesa estructuras muy densas, como huesos. Esto elimina radiaciones de baja energía, haciendo que el haz se vuelva más energético, lo que genera errores en los coeficientes de atenuación.
- Corrección:
- Uso de ecuaciones matemáticas o cortes más finos.
- Volumen parcial:
- Aparece cuando un vóxel incluye diferentes tejidos con coeficientes de atenuación muy dispares, lo que da lugar a un valor promedio que no refleja la realidad.
- Corrección:
- Reducción del grosor del corte.
- Artefactos en anillo:
- Producidos por un mal funcionamiento de uno de los detectores. Son característicos de equipos de tercera generación.
- Corrección:
- Verificación del sistema de control del equipo.
- Artefactos en estrella:
- Se generan al atravesar materiales muy densos como prótesis o clips quirúrgicos, causando rayas radiales alrededor del objeto.
- Corrección:
- Ajustes en el algoritmo de reconstrucción.
B) Artefactos de origen cinético
- Movimientos del paciente:
- Son los más comunes y ocurren por movimientos involuntarios durante el estudio.
- Corrección:
- Explicar al paciente la importancia de permanecer inmóvil.
- Usar inmovilizadores o sedación en niños o personas con dificultades para cooperar.
- Reducir los tiempos de exposición.
- Movimientos del sistema:
- Generados por vibraciones del sistema tubo-detectores o la mesa de exploración.
- Corrección:
- Inspección y reparación de los componentes mecánicos.
3. Uso del Catphan
- Descripción:
- El Catphan es un dispositivo que se coloca en la mesa del escáner y se utiliza para evaluar diferentes parámetros de calidad.
- Módulos y funciones:
- Amarillo (1.º módulo):
- Evalúa la exactitud de los números TC y los espesores de corte.
- Verde (2.º módulo):
- Mide la resolución espacial.
- Rojo (3.º módulo):
- Evalúa densidades y niveles de ruido.
- Azul (Base):
- Actúa como soporte sin funcionalidad directa.
- Amarillo (1.º módulo):
Conclusión
El control de calidad en TC, incluida la calibración diaria y la corrección de artefactos, es esencial para obtener imágenes precisas y confiables. La implementación rigurosa de estos procesos contribuye a diagnósticos más certeros y a la seguridad del paciente.
Otros controles de calidad en Radiología y Medicina Nuclear
Los controles de calidad en radiología y medicina nuclear son esenciales para garantizar imágenes diagnósticas de alta precisión, proteger a los pacientes y asegurar el funcionamiento adecuado del equipo. A continuación, se detallan los aspectos clave.
1. Controles de calidad en las unidades de revelado
- Limpieza del equipo:
- Es fundamental mantener limpio el equipo de revelado para evitar artefactos en las imágenes.
- Mantenimiento:
- Programado: Inspecciones regulares para prevenir fallos.
- Preventivo: Sustitución de componentes antes de que fallen.
- No programado: Reparaciones necesarias por fallos inesperados.
- Control diario:
- Verificar el funcionamiento y calibración del equipo.
2. Controles específicos en equipos de mamografía
Además de los controles estándar en equipos de radiografía, los de mamografía requieren:
- Control automático de exposición:
- Ajustes que aseguren una densidad óptica uniforme en las imágenes.
- Compresión de la mama:
- Garantizar una compresión adecuada, firme y tolerable.
- Cámara de imagen:
- Inspección de artefactos y resolución.
- Dosimetría:
- Medición de la dosis absorbida por el tejido para minimizar riesgos.
3. Controles en sistemas de registro y visualización
A) Sistemas analógicos
- Chasis y cartulinas:
- Revisión de limpieza y estado.
- Negatoscopios:
- Uniformidad del brillo y control de la intensidad lumínica.
- Cuartos oscuros y procesadoras:
- Limpieza y calibración periódica.
- Almacenamiento de películas:
- Mantener las condiciones adecuadas de temperatura y humedad.
B) Sistemas digitales
- Visualización y almacenamiento:
- Inspección de monitores, sistemas de archivo y recuperación de imágenes (PACS).
- Comprobación de la calidad de las imágenes en pantallas de diagnóstico.
4. Control de calidad en densitometría ósea
- Calibración diaria:
- Se realiza con fantomas que simulan densidades similares a las del tejido óseo.
- Fantomas específicos:
- Permiten evaluar la precisión del equipo en condiciones similares a las reales.
5. Control de calidad en Medicina Nuclear
A) Importancia
- En medicina nuclear, la calidad de las imágenes depende de:
- Distribución del radiofármaco en el cuerpo.
- Precisión de los equipos, técnicas y procesamiento utilizados.
B) Principios básicos
- Calidad física de las imágenes:
- Evaluación objetiva basada en índices específicos.
- Calidad clínica:
- Garantizar que las imágenes sean útiles para el diagnóstico.
C) Programa de control de calidad
- Evaluación regular:
- Detectar deterioros graduales que puedan comprometer la calidad de las imágenes.
- Identificar problemas obvios, como fallos en los fotomultiplicadores.
- Límites establecidos:
- Determinar cuándo un equipo no debe utilizarse.
- Considerar factores como la posibilidad de reparación, sustitución o el tipo de estudios a realizar.
- Procesos de control:
- Inspecciones diarias, semanales y mensuales para asegurar la calidad constante del equipo.
Beneficios de los controles de calidad
- Seguridad del paciente:
- Reducción de dosis innecesarias y artefactos en las imágenes.
- Optimización del diagnóstico:
- Obtención de imágenes claras y precisas.
- Mantenimiento de equipos:
- Extensión de la vida útil y reducción de costes por reparaciones inesperadas.
Glosario de términos en el control de calidad en Medicina Nuclear
- Exactitud:
- Definición: Estimación de la discrepancia entre el valor obtenido por un equipo o procedimiento y el valor verdadero o patrón calibrado.
- Aplicación: Permite determinar el error relativo de las medidas realizadas frente a un estándar reconocido.
- Precisión:
- Definición: Grado de consistencia o variabilidad de los valores obtenidos en un procedimiento de medida para una magnitud específica.
- Aplicación: Mide la reproducibilidad del proceso de medida, asegurando resultados consistentes en las mismas condiciones.
- Estabilidad:
- Definición: Capacidad de un equipo para mantener su funcionamiento constante a lo largo del tiempo y bajo diferentes condiciones operativas.
- Aplicación: Evalúa la fiabilidad del equipo en diferentes sesiones y periodos de trabajo.
- Resolución energética:
- Definición: Capacidad de un sistema detector de radiación para diferenciar entre energías cercanas.
- Aplicación: Es fundamental para obtener imágenes claras y separar señales de fondo y ruido.
- Ruido:
- Definición: Señales no deseadas que se manifiestan como granulado en las imágenes médicas.
- Aplicación: Su reducción es crucial para mejorar la calidad de la imagen y evitar interferencias diagnósticas.
- Artefactos:
- Definición: Falsas imágenes o alteraciones que no corresponden a la realidad del paciente, generadas por errores en el proceso técnico o por movimientos.
- Aplicación: Su identificación y corrección son esenciales para evitar diagnósticos erróneos.
- Sensibilidad:
- Definición: Capacidad del sistema para detectar señales de baja intensidad de radiación.
- Aplicación: Mejora la detección de lesiones pequeñas o cambios mínimos en las imágenes.
- Linealidad:
- Definición: Relación proporcional entre la respuesta del sistema y la cantidad de radiación recibida.
- Aplicación: Garantiza que las lecturas del equipo sean consistentes con los niveles reales de radiación.
- Uniformidad:
- Definición: Capacidad del sistema para proporcionar la misma respuesta a través de toda la superficie del detector.
- Aplicación: Evalúa la homogeneidad en las imágenes obtenidas, eliminando variaciones no deseadas.
- Calibración:
- Definición: Ajuste del equipo para asegurar que las mediciones sean precisas y correspondan a los valores reales.
- Aplicación: Realizado periódicamente, garantiza que el equipo cumple con los estándares requeridos.
- Resolución espacial:
- Definición: Capacidad del sistema para diferenciar objetos cercanos en una imagen.
- Aplicación: Influye directamente en la nitidez y claridad de los detalles anatómicos.
- Fidelidad:
- Definición: Grado en que una imagen obtenida representa con precisión la realidad del paciente.
- Aplicación: Asegura la confiabilidad de los diagnósticos basados en imágenes.
- Tiempo de respuesta:
- Definición: Tiempo que tarda un equipo en generar una imagen tras la adquisición de datos.
- Aplicación: Importante en situaciones clínicas donde la rapidez es crucial.
- Tasa de conteo:
- Definición: Número de eventos detectados por el sistema en un tiempo determinado.
- Aplicación: Evalúa la capacidad del sistema para procesar señales sin saturarse.
- Coeficiente de atenuación:
- Definición: Propiedad que mide cómo un material reduce la intensidad del haz de radiación.
- Aplicación: Se utiliza en la calibración y ajuste del sistema para obtener imágenes precisas.
- Ganancia:
- Definición: Relación entre la señal de salida y la señal de entrada en un detector.
- Aplicación: Optimiza el rendimiento del sistema para distintos niveles de energía.
- Artefactos cinéticos:
- Definición: Alteraciones en la imagen causadas por el movimiento del paciente o del equipo.
- Aplicación: Evitar mediante inmovilización adecuada o reducción de tiempos de exposición.
- Patrón de referencia:
- Definición: Un estándar contra el cual se comparan las medidas obtenidas.
- Aplicación: Asegura la coherencia entre distintos equipos y procedimientos.
- Volumen parcial:
- Definición: Artefacto causado por la presencia de tejidos con densidades diferentes dentro de un mismo vóxel.
- Aplicación: Se corrige ajustando el grosor del corte.
- Saturación:
- Definición: Estado en el cual un detector no puede procesar eventos adicionales por exceso de radiación.
- Aplicación: Prevenir configurando límites adecuados en el equipo.
Este glosario contiene términos fundamentales para comprender y aplicar el control de calidad en Medicina Nuclear, asegurando la precisión y confiabilidad en las imágenes diagnósticas.
Términos en Control de Calidad en Medicina Nuclear (Reescrito)
1. Resolución energética:
- Es la capacidad de un sistema detector de radiación para diferenciar entre fotones de energías similares. Se mide utilizando una fuente de energía monoenergética, evaluando la anchura a la mitad del máximo (FWHM, por sus siglas en inglés) del pico de energía registrado. Este valor se expresa en unidades de energía o en porcentaje relativo a la energía analizada.
2. Eficiencia de pico intrínseca:
- Es la fracción de fotones detectados entre los emitidos por la fuente que alcanzan el detector y depositan toda su energía en él. Esta medida incluye únicamente los eventos que generan un pico de energía total, representado como el área bajo dicho pico.
3. Respuesta en actividad:
- Es el análisis de la linealidad de la respuesta del sistema detector ante diferentes niveles de actividad radiactiva. Se expresa numéricamente mediante el coeficiente de correlación entre los valores de actividad y la respuesta del sistema.
4. Campo total de visión útil (CTVU):
- Es el área colimada que puede observar una gammacámara. Cuando no se utiliza colimador, corresponde a la longitud equivalente al 95% entre dos puntos opuestos que representan el 50% del recuento relativo al centro del cristal del detector.
5. Campo central de visión útil (CCVU):
- Corresponde al 75% de las dimensiones lineales del CTVU. Es una subregión central del campo total de visión útil.
6. Eficiencia:
- En pruebas de gammacámara, este término hace referencia a la capacidad del sistema para detectar e interpretar interacciones entre radiación y materia como eventos observables.
7. Pruebas intrínsecas:
- Se refieren a evaluaciones realizadas al sistema detector sin el uso de colimadores, evaluando únicamente las características propias del detector.
8. Píxel:
- Es el componente más pequeño de una imagen digital que contiene información. Su calidad determina el nivel de detalle y la nitidez de la imagen.
9. Falta de uniformidad integral (UI):
- Es una estimación global del cambio en la uniformidad de una imagen obtenida bajo una fuente homogénea de fotones. Se evalúa comparando el recuento de píxeles consecutivos y expresando la mayor diferencia como un porcentaje del total de recuentos.
10. Sensibilidad:
- Es la capacidad de un sistema de imágenes para transformar interacciones radiactivas en eventos observables. Se calcula como el cociente entre el número de eventos observados y la actividad de la fuente.
11. Resolución espacial:
- Es la capacidad del sistema para distinguir entre dos eventos que ocurren a corta distancia entre sí, visualizándolos como entidades separadas.
12. Resolución temporal:
- Es la habilidad del sistema para diferenciar entre dos impulsos sucesivos. Se mide como la tasa real de recuento a la que los impulsos detectados difieren de los impulsos incidentes en un 20%.
13. Prueba de referencia:
- Es un análisis exhaustivo de parámetros específicos del sistema. Su propósito es establecer un estándar con el que evaluar el rendimiento del equipo en pruebas futuras.
14. Prueba de constancia:
- Es una evaluación regular que asegura que el sistema mantiene condiciones óptimas de funcionamiento. Estas pruebas son menos complejas que las de referencia y pueden realizarse en un tiempo razonable.
Este conjunto de definiciones proporciona una comprensión clara y técnica de los términos clave utilizados en los controles de calidad dentro del ámbito de la Medicina Nuclear.
Normativa sobre criterios de calidad en Medicina Nuclear (Parafraseado)
Propósito y aplicación
- Esta normativa busca establecer estándares de calidad en Medicina Nuclear para garantizar una administración adecuada de los procedimientos y proteger la seguridad del paciente durante el uso de radiofármacos.
- Su ámbito de aplicación abarca todas las unidades asistenciales de Medicina Nuclear.
Programa de garantía de calidad
- Todas las unidades deben contar con un programa estructurado de garantía de calidad que cumpla con normativas nacionales o internacionales vigentes.
- Este programa incluirá:
- Procedimientos para garantizar una buena práctica clínica.
- Controles de calidad de los radiofármacos, los equipos y el tratamiento de datos.
- Evaluaciones de la dosis efectiva administrada por los radiofármacos empleados, así como parámetros para calcular la dosis absorbida por los pacientes.
- Descripción de los recursos humanos y materiales necesarios, con especificación de responsabilidades y niveles de autoridad.
- Este programa debe estar documentado y disponible para auditorías o revisiones por las autoridades competentes.
Responsabilidades del centro sanitario
- El centro deberá implementar el programa de calidad y designar un responsable para su creación, desarrollo y ejecución.
- Enviar una copia del programa a las autoridades sanitarias antes de comenzar actividades asistenciales.
- Mantener un registro anual de los resultados del programa.
- Nombrar un médico responsable, especializado en Medicina Nuclear.
Procedimientos clínicos
- Las unidades deben contar con protocolos escritos para optimizar la dosis absorbida por los pacientes durante los procedimientos médicos. Estos deben revisarse periódicamente y actualizarse cuando se introduzcan cambios o nuevas técnicas.
- Para calcular las dosis absorbidas, se emplearán los parámetros establecidos en el programa de calidad.
- En procedimientos que involucren mujeres en edad fértil, embarazadas o en periodo de lactancia, deben adoptarse medidas para minimizar riesgos. El médico evaluará cuidadosamente la necesidad del procedimiento.
- En la solicitud de estos procedimientos, debe incluirse información sobre el estado de embarazo o lactancia de la paciente.
- Solo personal cualificado y capacitado en protección radiológica puede llevar a cabo estas actividades.
Administración de radiofármacos
- La administración de radiofármacos con fines diagnósticos o terapéuticos debe realizarse bajo la supervisión de un especialista en Medicina Nuclear.
- En casos de administración incorrecta, el especialista designado en el programa de calidad estimará la dosis absorbida por el paciente lo antes posible, adoptando medidas para reducir los efectos y documentando las acciones realizadas en un informe.
- Si el caso es grave, el informe se remitirá al titular del centro y a las autoridades sanitarias.
Este marco normativo asegura que los procedimientos en Medicina Nuclear se realicen bajo altos estándares de calidad, garantizando la seguridad y efectividad en el manejo de radiofármacos.
Normativa sobre el uso de radiofármacos y procedimientos en Medicina Nuclear (Reformulación)
Administración de radiofármacos para fines diagnósticos
- El médico especialista es responsable de garantizar que la exposición del paciente a radiación sea mínima, sin comprometer la calidad del diagnóstico. También deberá tomar las medidas necesarias para evitar la repetición de pruebas por resultados insuficientes.
- Se debe seleccionar el radiofármaco más adecuado, utilizando la dosis óptima, especialmente en niños y pacientes con disfunción en algún órgano que afecte la absorción o eliminación del compuesto. Además, no se deben exceder los niveles máximos de actividad especificados para cada procedimiento y radiofármaco.
- En casos de radiofármacos no contemplados en los valores de referencia establecidos, se seguirán protocolos avalados por instituciones científicas nacionales o internacionales, incluyéndolos en el programa de calidad.
Administración de radiofármacos con fines terapéuticos
- En tratamientos con radiofármacos, el médico designado debe calcular la dosis recibida por los órganos más relevantes, considerando la distribución y eliminación del compuesto en el organismo.
Historia clínica
- Todo procedimiento con radiofármacos debe registrarse en la historia clínica del paciente, incluyendo:
- Tipo y cantidad de radionucleidos administrados.
- Información dosimétrica cuando sea pertinente.
- Incidencias de administraciones incorrectas.
- Reacciones adversas o efectos secundarios.
Uso en investigación clínica
- La administración de radiofármacos para investigación debe cumplir con los requisitos establecidos para ensayos clínicos con medicamentos.
- Se registrarán detalles del radiofármaco, actividad administrada y estimación de dosis absorbida en un informe específico.
Información al paciente
- Antes de un tratamiento con radiofármacos, el médico debe informar al paciente sobre posibles riesgos y medidas para minimizarlos. Asimismo, se entregará un documento de consentimiento informado que debe ser firmado.
- El paciente recibirá por escrito las instrucciones necesarias para proteger a las personas cercanas de la exposición a radiación.
- Esta información también será proporcionada a pacientes sometidos a procedimientos diagnósticos o que participen en investigaciones clínicas.
- Las mujeres serán advertidas sobre la necesidad de informar al especialista si están embarazadas o amamantando antes de proceder con la administración del radiofármaco.
Especialista en Radiofísica Hospitalaria
- Los centros con unidades de Medicina Nuclear deben contar con un especialista en radiofísica hospitalaria que participe en:
- Elaboración y optimización de programas de calidad en tratamiento de imágenes y datos.
- Control y mantenimiento de equipos de Medicina Nuclear.
- Gestión técnica y clínica de la dosimetría de radiación.
- Según la relevancia del centro, la autoridad sanitaria determinará si el especialista será parte del personal interno o si se recurrirá a servicios externos concertados.
Esta normativa asegura un control exhaustivo en el uso de radiofármacos y equipos de Medicina Nuclear, protegiendo la seguridad y bienestar de los pacientes y personal sanitario.
Normativa y Procedimientos Relativos a Equipos en Medicina Nuclear (Reformulación)
Pruebas de Aceptación del Equipamiento
- Todo equipo de Medicina Nuclear que entre en funcionamiento después de la aplicación de esta normativa debe pasar una prueba de aceptación previa.
- Estas pruebas, incluidas en las especificaciones de compra, deben ser realizadas por el proveedor del equipo en presencia de un representante técnicamente cualificado del comprador. Los resultados se documentarán en un informe que servirá como referencia para controles futuros.
- Las pruebas deberán garantizar que las características técnicas indicadas por el proveedor cumplen con los estándares establecidos y que los resultados son conformes con los niveles y tolerancias definidos en normativas nacionales o internacionales aplicables.
Programa de Control de Calidad
- Las unidades de Medicina Nuclear realizarán controles de calidad para garantizar que:
- Las dosis administradas a los pacientes sean las indicadas por el médico en tratamientos terapéuticos.
- En procedimientos diagnósticos, las dosis sean lo más bajas posibles sin comprometer la calidad de las imágenes.
- El control de calidad de los radiofármacos se regirá por la normativa aplicable y verificará que cumplen con los estándares para su uso médico.
- Los equipos empleados en Medicina Nuclear deberán someterse a pruebas regulares, ajustándose a protocolos avalados por organismos científicos o internacionales, que incluirán al menos las evaluaciones definidas en los anexos correspondientes.
- Los resultados de estos controles serán evaluados por un especialista en radiofísica hospitalaria, quien emitirá un informe sobre el estado del equipo y las anomalías detectadas. El médico responsable decidirá si las imágenes son aptas para el diagnóstico.
- En caso de anomalías significativas, el responsable de la unidad determinará si es posible continuar utilizando el equipo o si debe suspenderse su uso hasta que sea reparado.
Programa de Mantenimiento
- Cada unidad contará con un programa de mantenimiento preventivo y correctivo, que podrá ser realizado por el proveedor, el centro sanitario, o una empresa externa especializada.
- Tras cualquier reparación o intervención en el equipo, se realizará una verificación para asegurar que vuelve a funcionar correctamente. El proveedor deberá emitir un certificado confirmando la reparación.
- Si la intervención afecta la calidad de las imágenes o las dosis administradas, el especialista en radiofísica hospitalaria deberá verificar el estado del equipo y reportar los resultados al médico responsable, quien autorizará o no la reanudación de su uso.
- Los resultados de las verificaciones se compararán con las pruebas de aceptación iniciales o con registros previos de calidad.
Archivo de Documentación
- Los centros sanitarios deben conservar durante 30 años los informes relacionados con las pruebas clínicas y técnicas realizadas, así como los resultados de mantenimiento y controles de calidad.
- Los documentos relacionados con los equipos deberán mantenerse mientras dure su vida útil.
Historia de la Medicina Nuclear en España
La Medicina Nuclear en España tiene sus inicios en 1949, cuando el Dr. Blanco Soler y su equipo del Hospital de la Cruz Roja en Madrid comenzaron a diagnosticar enfermedades tiroideas utilizando radioisótopos. En esa época, debido a las limitaciones para obtener materiales radiactivos, se recuperaba y reutilizaba el radioyodo a partir de la orina de los pacientes previamente tratados.
Auditoría y Vigilancia en Medicina Nuclear
Artículo 16: Auditorías
Las autoridades sanitarias responsables implementarán un sistema de auditorías para evaluar si el programa de garantía de calidad en las unidades de Medicina Nuclear:
- Se ajusta a los objetivos establecidos.
- Cumple con las normativas aplicables.
- Se lleva a cabo de manera eficaz. Este proceso tiene como finalidad la certificación del cumplimiento de los estándares de calidad y normativas.
Artículo 17: Vigilancia
La autoridad sanitaria supervisará el cumplimiento de los criterios establecidos en el programa de control de calidad. Este seguimiento incluye:
- Proponer medidas correctivas en caso de encontrar deficiencias o problemas en los equipos o procedimientos.
- En situaciones donde no se adopten las medidas propuestas, la autoridad puede decidir clausurar provisional o definitivamente el equipo o la unidad de Medicina Nuclear.
Artículo 18: Infracciones y Sanciones
El incumplimiento de las disposiciones normativas será considerado una infracción administrativa en el ámbito sanitario. Dichas infracciones estarán sujetas a sanciones administrativas según lo estipulado en la legislación vigente y serán gestionadas mediante un procedimiento administrativo formal.
Otras Normativas Relacionadas
- Real Decreto 1132/1990, de 14 de septiembre: Establece las bases fundamentales de protección radiológica para las personas sometidas a tratamientos médicos.
- Directiva 2013/59/Euratom: Dicta las normas básicas de seguridad para proteger contra los riesgos derivados de la exposición a radiaciones ionizantes, reemplazando normativas previas.
- Ley 14/1986, de 25 de abril, General de Sanidad: Obliga a establecer requisitos mínimos para la acreditación de instalaciones de centros y servicios sanitarios, asegurando su eficacia y seguridad.
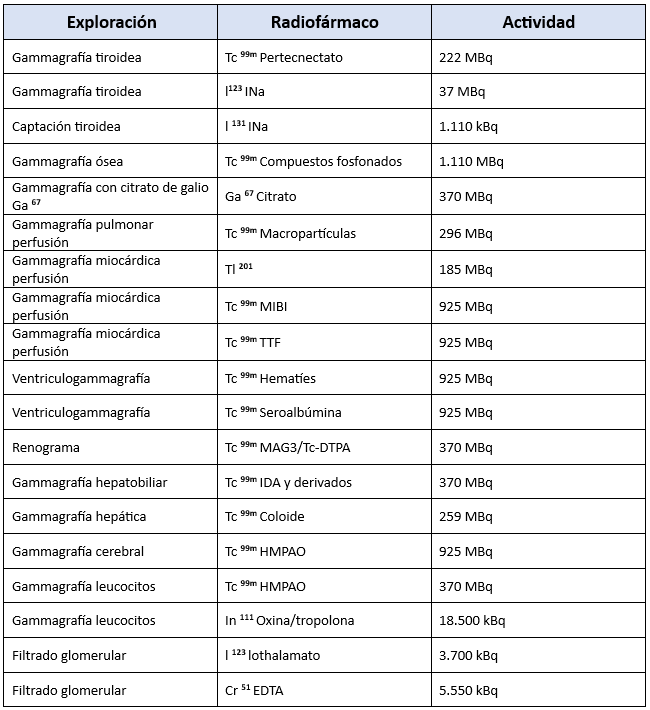
Actividades Máximas en Exploraciones y Radioterapias
El anexo correspondiente incluye una lista de las exploraciones más comunes en Medicina Nuclear, los radiofármacos utilizados, y las actividades máximas permitidas para cada procedimiento. Estas actividades se refieren a un paciente estándar y deben ajustarse considerando el tamaño corporal y la edad de cada individuo.
Para radiofármacos o exploraciones no incluidas en esta lista, el programa de garantía de calidad de cada unidad deberá incluir su propia referencia. Esta lista debe elaborarse siguiendo las recomendaciones de sociedades científicas y organismos competentes, asegurando el cumplimiento de las normativas aplicables.
Controles de Calidad en Medicina Nuclear: Equipamiento y Procedimientos
Exploraciones y Calidad del Equipamiento
Las exploraciones en medicina nuclear incluyen tanto exámenes planificadores como tomográficos o de cuerpo completo. Los controles de calidad se aplican a todos los equipos “in vivo” utilizados en el diagnóstico nuclear. Estos controles están diseñados para garantizar la precisión, estabilidad y funcionalidad de los equipos, asegurando la calidad diagnóstica y minimizando la exposición del paciente.
Requisitos Mínimos para el Control de Calidad
- Frecuencia y Documentación
- Las pruebas se realizarán con la periodicidad mínima indicada, documentadas por personal cualificado.
- Cambios en la periodicidad deben justificarse mediante protocolos reconocidos y reflejarse en el programa de garantía de calidad.
- Tras reparaciones, se realizarán pruebas específicas para garantizar el correcto funcionamiento.
- Especialista en Radiofísica Hospitalaria
- Efectuará al menos una revisión anual completa de los equipos, emitiendo un informe detallado sobre su estado.
Controles Específicos por Equipos
1. Activímetros
- Exactitud y Precisión: Los equipos deben tener una exactitud de ±10% y una precisión de ±5%, verificadas trimestralmente.
- Estabilidad: Comprobada diariamente con una tolerancia de ±5%.
2. Sistemas de Contaje “in vivo”
- Resolución Energética: Comprobada semestralmente, con un ancho a mitad de altura (AIMA) inferior al 10% para Cs-137.
- Eficiencia de Pico: Deberá ser superior al 60% para Cs-137, revisada trimestralmente.
- Linealidad: Evaluada trimestralmente para confirmar la respuesta proporcional a diferentes actividades.
3. Gammacámara Planar
- Uniformidad Extrínseca: Analizada semanalmente, con valores de uniformidad integral (UI) y diferencial (UD) inferiores al 10%.
- Sensibilidad: Medida mensualmente, con un valor relativo mayor al 80% y un valor absoluto superior a 100 cps/MBq.
- Resolución Espacial: Comprobada mensualmente utilizando una fuente lineal, con desviaciones dentro del ±5% de los valores del fabricante.
- Resolución Energética: Revisada semestralmente; el AIMA del Tc-99m no debe diferir en más del 10% del valor especificado.
- Resolución Temporal: Verificada semestralmente para tasas de recuento con pérdida del 20%, asegurando que no disminuya más del 10% del valor especificado.
- Tamaño del Píxel: Los tamaños en los ejes X e Y no deben diferir más del 5%, revisado semestralmente.
Condiciones Generales para Pruebas
- Radionucleido de Elección: Generalmente Tc-99m, aunque se puede usar Co-57 en pruebas prácticas.
- Tasa de Cuentas: Recomendación de no superar los 10,000 cps para pruebas de sensibilidad.
- Imagen Analizada: Incluye los campos de visión total y central.
- Colimador Habitual: Usado para pruebas extrínsecas, verificando variaciones en resolución y sensibilidad.
Conclusión
El mantenimiento de la calidad en los equipos de medicina nuclear es esencial para garantizar diagnósticos fiables, minimizar riesgos y cumplir con los estándares de protección radiológica. Estos controles específicos aseguran la eficiencia y precisión de los procedimientos, protegiendo al paciente y optimizando los recursos del servicio médico.
Controles de Calidad en Cámaras Tomográficas y Radioinmunoanálisis (RIA)
Cámaras Tomográficas
Las gammacámaras diseñadas para estudios tomográficos deben cumplir con los mismos estándares que las cámaras planas y superar pruebas específicas adicionales que aseguren su correcto funcionamiento en la modalidad tomográfica.
- Uniformidad Planar
- Debe realizarse mensualmente, o con mayor frecuencia según las instrucciones del fabricante.
- Esta prueba es fundamental para programas de reconstrucción tomográfica.
- Se requiere adquirir un mínimo de 10,000 cuentas por píxel para garantizar una evaluación adecuada.
- Centro de Rotación
- Evaluado mensualmente siguiendo las especificaciones del fabricante.
- La desviación no debe exceder la mitad del tamaño del píxel más pequeño utilizado en las imágenes.
- Uniformidad Tomográfica
- Mensualmente se adquieren imágenes de un maniquí cilíndrico de al menos 20 cm de diámetro.
- Estas imágenes no deben presentar artefactos visibles, como anillos, que puedan indicar irregularidades en el sistema.
Radioinmunoanálisis (RIA)
El RIA es una técnica “in vitro” utilizada principalmente en endocrinología para analizar muestras biológicas y medir concentraciones hormonales específicas. Esto se realiza mediante reacciones entre antígenos y anticuerpos, apoyadas en técnicas de detección de radiación.
Generalidades
- Se basa en la interacción de antígenos y anticuerpos para la cuantificación hormonal.
- Los reactivos utilizados suelen ser productos comerciales diseñados para este propósito.
- Requiere un riguroso control de calidad para garantizar resultados fiables.
Tipos de Controles
- Controles Externos
- Involucran reactivos comprados a laboratorios especializados.
- Los laboratorios envían patrones con valores ya cuantificados.
- Se realiza una curva en el servicio, que se compara con los estándares del fabricante.
- Aspectos evaluados:
- Precisión: Puede ser afectada por errores técnicos en el diseño o fallos operativos.
- Exactitud: Determina si los valores obtenidos son consistentes con los reales.
- Sensibilidad: Mide la capacidad de detectar pequeñas variaciones en las concentraciones.
- Controles Internos
- Se realizan diariamente en el laboratorio para garantizar que todo el material utilizado esté en óptimas condiciones.
- Material del paciente: Se verifica si las muestras están en buen estado comparando actividades relativas.
- Contador de Centelleo:
- Verificar el nivel base en un tubo vacío.
- Calibrar el voltaje máximo del tubo fotomultiplicador utilizando un patrón conocido.
Conclusión
Estos controles son fundamentales para asegurar la precisión diagnóstica y la calidad en los procedimientos realizados con gammacámaras tomográficas y en técnicas de radioinmunoanálisis. Al mantener protocolos estrictos, se garantiza la fiabilidad de los resultados y la seguridad de los pacientes.
Control de Calidad de los Radiofármacos
Conceptos Generales
El control de calidad de los radiofármacos (RF) es fundamental para garantizar su uso seguro y efectivo. Existen tres objetivos clave en este proceso:
1. Eficacia: Asegurarse de que el radiofármaco cumpla con el propósito para el que fue diseñado.
2. Seguridad: Garantizar que no cause daño al paciente.
3. Pureza del producto: Verificar que el radiofármaco esté libre de contaminantes o impurezas que puedan afectar su efectividad o seguridad.
Pruebas Habituales de Pureza
Las pruebas de calidad que se realizan para asegurar la pureza de los radiofármacos incluyen:
1. Pruebas físico-químicas: Evaluación de aspectos como apariencia, color, tamaño, número de partículas, pH y ausencia de elementos extraños.
2. Pruebas biológicas: Comprenden estudios de esterilidad, toxicidad y apirogenicidad (ausencia de sustancias que puedan causar fiebre).
3. Otras pruebas específicas: Aplicadas dependiendo del entorno, ya sea hospitalario o industrial.
Control de la Pureza Radioquímica y Radionucleídica
- Pureza Radionucleídica (PRN):
- Evalúa la proporción entre la actividad de un radionúclido específico y la actividad total del radiofármaco.
- Causas de impurezas radionucleídicas:
- Producción: Problemas como pH inadecuado del eluato o daño en la columna de alúmina del generador.
- Decaimiento radiactivo: Uso excesivo del generador que produce acumulación de Mo-99.
- Efectos adversos:
- Imágenes de baja calidad.
- Exposición innecesaria a radiación.
- Técnicas de control:
- Uso de blindajes específicos para distinguir entre las radiaciones gamma y beta de Mo-99 y Tc-99m.
- Espectrofotometría de alta sensibilidad.
- Pureza Radioquímica (PRQ):
- Determina el porcentaje de actividad que corresponde a la forma química deseada.
- Causas de impurezas radioquímicas:
- Preparación incorrecta del radiofármaco.
- Interacción con agentes químicos en el disolvente.
- Cambios en temperatura o pH.
- Efectos adversos:
- Formación de depósitos en tejidos no deseados.
- Imágenes diagnósticas de menor calidad.
- Técnicas de control:
- Cromatografía en papel o capa fina para separar y analizar componentes químicos.
- Control del disolvente y uso de aditivos para prevenir reacciones químicas indeseadas.
Recomendaciones
Los límites de pureza y los métodos de control son definidos por estándares internacionales, como la Farmacopea Europea, y varían según el radiofármaco en cuestión. Es esencial garantizar que estos parámetros se cumplan para evitar problemas durante su aplicación clínica.
Control de Calidad del Generador de Molibdeno/Tecnecio
A) Conceptos Generales
El Tecnecio-99m (Tc-99m) es el radionúclido más utilizado en diagnóstico médico nuclear debido a sus propiedades favorables. Sin embargo, es esencial garantizar que el eluato, que es el líquido obtenido del generador, cumpla con ciertos estándares de calidad. Esto asegura que el radiofármaco resultante sea seguro y eficaz.
El control del generador se centra en tres áreas principales:
1. Control físico-químico: Evalúa aspectos como el pH y la presencia de impurezas.
2. Control radiológico: Asegura la pureza del radionúclido y su forma química.
3. Control biológico: Verifica la ausencia de agentes contaminantes, como pirogénicos o bacterias.
B) Control Físico-Químico
Este tipo de control incluye las siguientes verificaciones:
- Apariencia del eluato:
- El eluato debe ser transparente y no presentar partículas en suspensión ni turbidez.
- pH del eluato:
- El valor promedio aceptable es de 5,5, aunque se permite un rango entre 4,5 y 7.
- Se mide mediante tiras de papel indicador que cambian de color en función del pH.
- Contenido de aluminio:
- La presencia de aluminio en el eluato puede interferir en la preparación del radiofármaco.
- Se detecta mediante pruebas colorimétricas utilizando papel indicador.
- El límite máximo permitido es de 10 ppm (partes por millón).
C) Control Radiológico
Este apartado verifica aspectos clave del radionúclido:
- Pureza radionucleídica (PRN):
- Confirma que el radionúclido presente corresponde al deseado (Tc-99m) y que no hay contaminantes como Mo-99 en cantidades superiores a lo permitido.
- Pureza radioquímica (PRQ):
- Asegura que el Tc-99m está en su forma química adecuada para su uso clínico.
Ambos controles han sido descritos previamente y son esenciales para garantizar la eficacia y seguridad del producto.
D) Control Biológico
Este control asegura que el eluato no contiene contaminantes biológicos que puedan causar daño al paciente. Se centra en:
- Apirogenicidad:
- Evalúa la ausencia de pirogénicos (sustancias que causan fiebre).
- Este control se realiza principalmente cuando el volumen de disolución a administrar supera los 15 ml.
- Métodos utilizados:
- Método del conejo: Evalúa la reacción en conejos tras la administración.
- Método del lisado de amebocitos: Detecta pirogénicos en muestras líquidas con alta sensibilidad.
- Esterilidad:
- El generador se esteriliza en fábrica mediante autoclave, aplicando vapor a alta presión y temperatura (120°C durante 15-20 minutos).
- Además, se incorpora un filtro esterilizador al sistema.
- El control de esterilidad se realiza de forma aleatoria mediante muestreo, seleccionando unidades de generadores para un análisis microbiológico riguroso.
Estos procedimientos garantizan que el generador de Molibdeno/Tecnecio cumpla con los estándares de seguridad y calidad para su uso médico.
Control de calidad y mantenimiento del tomógrafo PET
Concepto
El control de calidad del tomógrafo PET incluye un conjunto de pruebas diseñadas para evaluar su funcionamiento, simulando condiciones similares a las de un estudio con pacientes. Estas pruebas permiten detectar y corregir errores, asegurando un rendimiento óptimo del equipo.
Tipos de Pruebas
Se realizan principalmente dos tipos de pruebas:
- Prueba de estabilidad o uniformidad del equipo:
- Evalúa la homogeneidad o uniformidad de la respuesta de los detectores antes de iniciar el uso diario del tomógrafo.
- Se compara la eficiencia de los detectores actuales con valores de referencia previamente establecidos.
- Procedimiento:
- Adquisición en blanco: Se realiza un estudio en 2D con una fuente de transmisión que garantiza una estadística suficiente (mínimo 30.000 cuentas).
- Adquisición en blanco de referencia: Es una medición previa realizada tras la última normalización del equipo.
- Parámetros evaluados:
- Diferencias entre los bloques detectores respecto a los valores de referencia. Si la diferencia supera el 10 %, se considera un error.
- Número de bloques detectores que tienen una variación superior a 3 desviaciones estándar.
- Varianza entre la medición actual y la referencia.
- Periodicidad: Esta prueba debe realizarse diariamente.
- Prueba de funcionamiento del tomógrafo PET:
- Comparación de las prestaciones del equipo actual con las de referencia.
- Técnicas evaluadas:
- Mediciones básicas intrínsecas:
- Resolución espacial.
- Fracción de coincidencias espaciales.
- Sensibilidad del equipo.
- Pérdida de cuentas debido al tiempo muerto y a coincidencias aleatorias.
- Corrección de efectos físicos:
- Uniformidad en la reconstrucción tomográfica.
- Corrección de radiación dispersa.
- Corrección por atenuación y linealidad en la tasa de recuento.
- Mediciones básicas intrínsecas:
Periodicidad de las Pruebas
- Pruebas sistemáticas: Se realizan cada 9 meses, considerando la semivida de la fuente radiactiva de germanio-68 (Ge-68), que es de aproximadamente 9 meses. La reposición de esta fuente se realiza cada 12-18 meses.
- Pruebas por incidencias: Se efectúan cuando aparecen problemas en la calidad de los detectores, normalmente asociados a averías.
Personal Responsable
Estas pruebas son realizadas por el personal técnico especializado del tomógrafo, garantizando que las mediciones cumplan con los estándares requeridos.
Averías en el sistema PET
Las averías en las instalaciones de un sistema PET pueden clasificarse en los siguientes tipos:
a) Alteraciones en el control de calidad diario
Estas ocurren cuando el monitoreo de los detectores muestra valores fuera de los límites normales. En tales casos, se debe notificar al servicio técnico para realizar las correcciones necesarias.
b) Problemas en el sistema de control de temperatura
El correcto funcionamiento del sistema de refrigeración es esencial para mantener la temperatura adecuada en diferentes áreas. Se debe supervisar continuamente la temperatura en los siguientes lugares:
1. Gantry: Requiere un sistema de enfriamiento por agua (Water-Chiller) para mantener una temperatura constante de 18 °C.
2. Sala de exploración: La temperatura no debe superar los 28 °C.
3. Sala de control: La temperatura también debe permanecer por debajo de 28 °C.
En caso de un aumento excesivo de temperatura, se activarán alarmas audiovisuales. Si no se detecta a tiempo, el equipo podría detenerse y sufrir daños.
c) Fallos eléctricos o cortes de suministro
Estos ocurren cuando hay una interrupción repentina en el suministro eléctrico, como un apagón. En estos casos, los comandos del gantry pueden bloquearse. Los pasos para solucionar esta situación son los siguientes:
- Revisar la fuente radiactiva de germanio-68:
- Asegurarse de que esté retraída. Si no es así, se debe impedir el acceso a la sala y retraerla automáticamente desde la consola en la sala de control.
- Desbloquear la camilla:
- Colocar la camilla en la posición “0”.
- Desbloquear los septos:
- Presionar el botón correspondiente en el control del gantry.
- Verificar la conexión:
- Confirmar que la torre está conectada al sistema de adquisición del tomógrafo (ACS).
Prevención de averías
Es fundamental realizar un monitoreo constante del funcionamiento durante los estudios para prevenir problemas. Esto incluye supervisar al paciente y el desarrollo de la exploración, identificando cualquier incidente que pueda surgir.
Control de calidad en estudios SPECT
La calidad en los estudios SPECT, como en cualquier procedimiento de Medicina Nuclear, depende de todos los pasos involucrados en la obtención de imágenes, incluyendo:
- Calidad de los radiofármacos: Es esencial que sean de alta pureza y eficacia.
- Estado del paciente: Debe estar en condiciones óptimas para minimizar movimientos y obtener mejores resultados.
- Resolución del sistema utilizado: Depende del equipo y los ajustes realizados.
- Parámetros de adquisición:
- Órbitas de obtención.
- Tipo de colimadores.
- Configuración del sistema.
Factores específicos del SPECT
Este tipo de estudio, una variante avanzada de la gammacámara, requiere la optimización de los siguientes parámetros:
- Resolución:
- Determinada por la resolución planar del sistema.
- Influenciada por:
- Uso de un colimador de alta resolución.
- Reducción de la distancia entre el cabezal y el paciente (radio de órbita).
- Tamaño del píxel en la matriz utilizada.
- Contaje:
- Se refiere al número de fotones detectados por la cámara. Un mayor contaje mejora la resolución de manera indirecta.
- Factores que lo afectan:
- Dosis administrada (cantidad de fotones gamma emitidos).
- Número de proyecciones realizadas.
- Tiempo de adquisición de las proyecciones.
- Diseño del colimador.
- Número de cabezales detectores.
Control de Calidad y Normas de Seguridad en Resonancia Magnética (RM)
Normativas Internacionales Aplicables a Instalaciones de RM
Aunque a nivel nacional no existe una normativa específica para instalaciones de RM, las directrices internacionales son orientadas principalmente por la FDA (Food and Drug Administration) de los Estados Unidos. Estas recomendaciones abarcan los siguientes aspectos:
- Campo Magnético Estático
- Los campos magnéticos estáticos con intensidades inferiores a 2 teslas se consideran seguros. Si el equipo supera este nivel, el fabricante debe garantizar medidas adicionales para asegurar la seguridad.
- Campo Magnético de Gradiente
- La exposición a campos magnéticos variables en el tiempo debe limitarse para evitar posibles efectos adversos, como la estimulación nerviosa.
- Niveles de Ruidos Acústicos
- Los ruidos generados durante el procedimiento deben mantenerse dentro de niveles aceptables. La FDA recomienda valores entre 65 dB y 95 dB. Como medida de protección, se deben proporcionar elementos como tapones auditivos o auriculares.
Normas Generales de Seguridad para la RM
Para garantizar la seguridad y comodidad de los pacientes durante el procedimiento, se deben seguir ciertas pautas:
- Señalización de Seguridad
- Es esencial colocar señales de advertencia visibles en la entrada de la unidad y dentro de la sala de exploración. Estas señales deben alertar sobre los posibles efectos del campo magnético en implantes electrónicos, dispositivos metálicos o cualquier objeto ferromagnético. También se deben advertir los riesgos para dispositivos electrónicos como tarjetas bancarias, teléfonos móviles o cámaras.
- Restricción de Acceso
- La sala de exploración debe tener acceso restringido. Solo personal autorizado puede ingresar, y se debe controlar el ingreso de materiales metálicos.
- Cuestionario de Seguridad
- Antes de realizar el estudio, el paciente debe completar un cuestionario o firmar un consentimiento informado. Este cuestionario tiene como propósito identificar:
- Implantes metálicos internos o externos.
- Dispositivos sensibles al electromagnetismo, como marcapasos o bombas de medicación.
- Intervenciones quirúrgicas previas que puedan haber incluido implantes metálicos o grapas.
- Cuerpos extraños metálicos, especialmente en los ojos. En caso de sospecha, se debe realizar una radiografía para descartarlos.
- También se debe registrar si la paciente está embarazada o si tiene antecedentes alérgicos relevantes en caso de que se requiera la administración de contraste intravenoso.
- Antes de realizar el estudio, el paciente debe completar un cuestionario o firmar un consentimiento informado. Este cuestionario tiene como propósito identificar:
Importancia del Cuestionario
El cuestionario actúa como un filtro de seguridad, ayudando al personal médico a identificar riesgos potenciales y definir responsabilidades antes de iniciar el estudio. Además, contribuye a minimizar posibles complicaciones relacionadas con la interacción del campo magnético con objetos o dispositivos sensibles en el paciente.
Acceso de Material Paraclínico en Resonancia Magnética (RM)
Es importante verificar que el material utilizado en la sala de RM no contenga componentes ferromagnéticos, para garantizar la seguridad y evitar interacciones con el campo magnético. Entre estos materiales, se incluyen:
- Sillas de ruedas y camillas utilizadas para el transporte de pacientes.
- Soportes de suero y utensilios especiales requeridos por algunos pacientes.
- Equipos médicos portátiles, como bombas de infusión de medicamentos y carros de anestesia.
Sistema de Intercomunicación con el Paciente
La comunicación constante con el paciente durante el examen es esencial. Para ello:
- Contacto visual y auditivo: El equipo de RM debe estar equipado con un sistema de intercomunicación que permita al técnico mantenerse en contacto con el paciente.
- Timbre de emergencia: El paciente debe tener acceso a un timbre que pueda activar en caso de necesidad. Esto asegura que pueda alertar al personal sanitario ante cualquier eventualidad.
- Antes del examen, el paciente debe ser informado sobre el procedimiento y las medidas de seguridad, lo que fomenta su colaboración y reduce posibles tensiones o incertidumbres.
Contraindicaciones Absolutas para RM
Hay ciertas condiciones que hacen imposible realizar un examen de RM de manera segura, como:
- Implantes electrónicos:
- Marcapasos.
- Estimuladores nerviosos.
- Implantes cocleares.
- Presencia de materiales metálicos:
- Clips vasculares en aneurismas cerebrales.
- Prótesis óseas metálicas.
- Fragmentos metálicos en tejidos blandos o intraoculares.
- Prótesis o fragmentos magnéticos:
- Aquellos con propiedades ferromagnéticas que puedan moverse con el campo magnético y causar daños a estructuras vitales.
Normas de Seguridad Relacionadas con Refrigerantes en RM Superconductivas
Los imanes superconductores utilizan helio líquido como refrigerante para mantener la corriente eléctrica circulando sin resistencia y garantizar la funcionalidad del sistema. Algunas medidas clave son:
- Gestión del helio líquido:
- El helio se utiliza para mantener la superconducción necesaria en los imanes.
- En caso de pérdida de superconducción (conocida como “quench”), el helio puede evaporarse rápidamente, causando daños al equipo y poniendo en riesgo al personal.
- Manejo especializado:
- El manejo del helio debe ser realizado exclusivamente por personal especializado.
- Es necesario revisar periódicamente los contenedores de helio, siguiendo las recomendaciones del fabricante.
- Los proveedores autorizados o el fabricante mismo suelen encargarse de estas tareas para garantizar el correcto funcionamiento del equipo.
Estas normas buscan proteger tanto la integridad del equipo de RM como la seguridad de los pacientes y del personal médico.
Características del Helio como Refrigerante
El helio es un gas que no tiene olor, no es inflamable ni tóxico, y no causa irritaciones. Sin embargo, en contacto directo puede provocar quemaduras por frío extremo debido a su baja temperatura. Aunque no es peligroso por sí mismo, puede generar riesgo de asfixia al desplazar el oxígeno en el aire, reduciendo su concentración y dificultando la respiración.
Efectos del Helio sobre las Personas
1. Asfixia: La disminución del oxígeno en el aire por desplazamiento de las moléculas de oxígeno puede causar asfixia en entornos con helio.
2. Quemaduras por congelación: El contacto directo con helio líquido o helio enfriado puede producir lesiones severas por frío.
Medidas de Control de Calidad en Resonancia Magnética
Además de las normativas que regulan los campos magnéticos, los refrigerantes y el material paraclínico, existen procedimientos específicos de control de calidad para otros elementos en Resonancia Magnética:
- Antenas de radiofrecuencia: Estas requieren verificaciones periódicas para garantizar una correcta emisión y recepción de las señales.
- Calidad de las imágenes: Las pruebas deben confirmar que las imágenes cumplen los estándares necesarios para el diagnóstico.
- Sistemas informáticos y software: Se debe garantizar el correcto funcionamiento del software y los equipos informáticos asociados.
- Tecnologías complementarias: Incluyen sistemas de impresión y otros dispositivos utilizados en los estudios de RM.
Por lo general, estos controles específicos son realizados por las empresas proveedoras de los equipos, según las características particulares de cada dispositivo.
Mantenimiento de Equipos
Es responsabilidad del operador garantizar un servicio seguro, eficaz y respetuoso con el entorno. Esto incluye:
1. Protección del medio ambiente y la población: Asegurar que el uso de los equipos no implique riesgos para el entorno ni para las personas.
2. Eficiencia de los sistemas de protección: Comprobar periódicamente los dispositivos de seguridad para la radiación y garantizar su buen funcionamiento.
3. Autorizaciones y controles: Antes de poner en marcha cualquier equipo, es necesario realizar evaluaciones desde la perspectiva de protección radiológica.
4. Calibración periódica: Los instrumentos de medición deben ser ajustados regularmente para asegurar resultados precisos.
Responsabilidad del Mantenimiento
Aunque el mantenimiento suele ser realizado por los fabricantes de los equipos o empresas especializadas, existen algunas tareas específicas que pueden ser llevadas a cabo por el personal técnico del centro, como:
- Verificación del estado general de los equipos.
- Realización de controles básicos de funcionalidad.
- Notificación de incidencias que requieran intervención externa.
Estas acciones garantizan el uso continuo y seguro de los equipos en el diagnóstico por imágenes y medicina nuclear.


