3. GESTIÓN DE RESIDUOS SANITARIOS. CLASIFICACIÓN, TRANSPORTE, ELIMINACIÓN Y TRATAMIENTO.
3.1. CLASIFICACIÓN
La clasificación de residuos se realiza según el tipo de residuo que se genere, siendo el personal que trabaja en los distintos servicios el encargado de identificar los residuos que produce, segregarlos y envasarlos para su posterior eliminación. De ahí la importancia de saber identificar y diferenciar los distintos tipos de residuos.
3.1.1. Residuos no peligrosos:
Se impone la recogida selectiva para disminuir el volumen de residuos que se depositen en vertederos
– Grupo I: residuos generales asimilables a urbanos: son los que se producen fuera de la actividad asistencial (comedores, salas administrativas, salas de espera, etc.).
Se recogen en bolsa de color negro (normativa UNE 53-147-85 y de un mínimo de 200 galgas), las repone y retira el servicio de limpieza.
– Grupo II: residuos sanitarios asimilables a urbanos: son los que se producen por la actividad asistencial y/o de investigación asociada, que no están incluidos entre los considerados como residuos sanitarios peligrosos. Se producen en todos los lugares donde se realice atención sanitaria. Se recogen en bolsa de color marrón, en bolsa (normativa igual que la anterior) no mayor de 60 litros. Son cerradas, retiradas y repuestas por el servicio de limpieza.
3.1.2. Residuos peligrosos
– Grupo III A. Residuos peligros sanitarios.
– Grupo III B. Residuos químicos y citostáticos.
– Grupo IV. Residuos radiactivos.
– Grupo V. Residuos peligrosos de origen no sanitario.
Estos residuos contienen sustancias que pueden representar un peligro para el medio ambiente, la salud humana o los recursos naturales. Están identificados con un asterisco en la Lista
Europea de Residuos (LER), y la finalidad de esta ley es la de ayudar a clasificar los residuos en función de su origen y naturaleza.
Codificación según R.D. 833/1988 y R.D.952/1977. Para la identificación de los residuos peligrosos se les asigna un código compuesto por 7 dígitos, cada uno de los cuales caracterizan el residuo y facilita su control desde que se produce hasta su destino final. El código nos aporta la siguiente información:
– La razón por la que hay necesidad de que sea gestionado (productor).
– Cómo va ser gestionado (gestor).
– El tipo de genérico o categoría a la que pertenece su estado físico: líquido, lodo, sólido y gas licuado o comprimido (productor).
– Principales constituyentes (fichas de datos de seguridad/caracterización).
– La actividad que lo genera (productor).
– El proceso generador del mismo (productor).
Etiquetado de los residuos. Deberán estarlo de forma clara, legible e indeleble y al menos en la lengua española. Debe figurar:
– El código de identificación del residuo.
– Nombre, dirección y teléfono del titular del residuo.
– Fecha de envasado. Indica el comienzo del almacenamiento. Este tiempo de almacenamiento no podrá exceder de 6 meses.
– La naturaleza de los riesgos que presenta el residuo.
– La etiqueta se fijará firmemente al envase y se anularán las anteriores para evitar confusiones.
– Se deben imprimir con los pictogramas correspondientes, en negro sobre fondo amarillo-naranja.
3.1.2.1. Grupo III A. Residuos peligrosos sanitarios
Son los producidos en la actividad asistencial y/o de investigación asociada, que conlleva algún riesgo potencial para los trabajadores expuestos o para el medio ambiente, o por razones de ética o estética, siendo necesario observar medidas de prevención en su manipulación, recogida, almacenamiento, transporte, tratamiento y eliminación.
Están constituidos por residuos de pacientes con infecciones altamente virulentas y erradicadas, residuos de pacientes con infecciones de transmisión oral-fecal, por aerosoles, filtros de diálisis de pacientes infecciosos, residuos punzantes y cortantes independientemente de su origen, cultivos y reservas de agentes infecciosos, residuos de animales infecciosos de experimentación, cantidades importantes de líquidos corporales, especialmente sangre humana, residuos anatómicos humanos reconocibles. Se desglosan en:
a) Infecciosos.
b) Material cortante/punzante. Se depositan en contenedores de un máximo de 3 litros.
c) Cultivos y reservas de agentes infecciosos, se incluyen los residuos de pacientes en diálisis con virus VHC, VHB, VIH.
d) Residuos infecciosos de animales de experimentación, y material en contacto con ellos.
e) Vacunas vivas y atenuadas. Viales y jeringas con restos y las vacunas caducadas.
f) Sangre y hemoderivados de forma líquida. En cantidades mayores a 100 ml, la orina se vierte en el desagüe y el envase a la basura (RSAU).
g) Residuos anatómicos no identificables. Procedentes de exéresis quirúrgicas, placentas, piezas anatómicas sin formol… Se recogen en bolsas de color rojo que cumplan la normativa UNE 53-147- 85, con galga mínima de 400, preferentemente de material reciclado, y en contenedores reutilizables o de un solo uso (en ese caso no será necesaria la bolsa), de color verde de 60 litros.
Los residuos considerados M.E.R. (Material Específico de Riesgo), en contenedores azules y se añadirá una etiqueta con la leyenda incineración.
3.1.2.2. Grupo III B. Residuos químicos y citostáticos
Es el material de desecho contaminado con productos de naturaleza química.
1. Medicamentos citotóxicos y citostáticos
Incluyen los medicamentos y las excretas de los pacientes que los han recibido. Estos residuos presentan propiedades mutagénicas, teratógenas y cancerígenas que pueden producir efectos locales irritantes, vesicantes y alérgicos.
Principios de eliminación: la principal premisa es la de evitar el residuo, para ello se realizará una producción centralizada. Facilitar un mejor conocimiento y aprendizaje. Favorecer la instauración de circuitos de detección de errores, lo que lleva a una mejor calidad del producto y seguridad de los técnicos.
Almacenaje: se realizará en el servicio de Farmacia, en los servicios donde se tenga que administrar solo estará las unidades de administración inmediata, el personal conocerá las propiedades de estos productos, estar en dispositivos que prevengan roturas y limiten la extensión de fugas, deben estar separadas del resto de medicamentos.
Deben prepararse en campana de flujo laminar vertical, protegiéndose con guantes, bata y mascarilla, desechando los residuos en el contenedor con su bolsa adecuada. Contenedor de color rojo, volumen máximo de 60 litros, con bolsa roja. Son de un solo uso, están elaborados con materiales rígidos, impermeables, resistentes a agentes químicos y materiales perforantes, disponen de cierre provisional que garantiza la estanqueidad hasta el llenado y con cierre hermético provisional. Una vez finalizado su uso debe identificarse como “RESIDUO CITOTÓXICO”.
2. Residuo de origen químico
Existen diversos tipos:
– Medicamentos desechados. No son considerados peligrosos pero son sometidos a recogida selectiva. Se incluyen los caducados, restos y los que se han alterado por cualquier causa.
– Residuos líquidos: líquido revelador o similar de las radiografías, desinfectantes a base de aldehídos. Otros no sanitarios pero que se producen en su actividad: aceites usados, disolventes, productos químicos, etc.
– Mercurio. Están en materiales de medida (termómetros, etc.), pilas de botón y algunas lámparas.
– Reactivos de laboratorio. Se clasifican a su vez en:
• Disolventes halogenados. Contienen más del 2% de algún halógeno.
• Son muy tóxicos e irritantes, en algunos casos cancerígenos (cloroformo, cloruro de metileno, etc.).
• Disolventes no halogenados: líquido orgánico inflamable que contenga menos del 2% de un halógeno. Son inflamables y tóxicos. Evitar mezclas con productos que no sean insolubles (etanos, metanol, etc.).
• Disoluciones acuosas. Soluciones acuosas de productos orgánicos e inorgánicos.
• Ácidos. Ácidos inorgánicos y soluciones acuosas de concentraciones mayores del 10%. Hay que tener precaución pues pueden tener reacciones de incompatibilidad.
• Aceites. Aceites minerales derivados de mantenimiento y calefactores.
• Sólidos: parafina, carbón activo…
• Especiales. Reactivos caducados y obsoletos. No deben mezclarse entre si no con los de otro grupo.
• Mezclas. Se tratarán como el producto más peligroso de los que contenga la mezcla, o que tengan simultáneamente consideración de dos grupos diferentes, (restos anatómicos conservados en formol se considerarán residuo III A y III B y se etiquetarán conforme a lo dispuesto en cada uno de los grupos.
• Sustancias clasificadas como cancerígenas o mutagénicas.
• Recipientes y envases. Todos los hayan contenido restos del grupo III B.
Fichas de datos de seguridad. Contendrán información sobre los productos que contiene, con lo que va a facilitar su clasificación sin tener que analizarlo. La clase de residuo y su peligrosidad va a depender del tipo de sustancias que lo componen y la concentración del preparado que forman.
Sustancias: son elementos químicos y sus compuestos en estado natural, o los obtenidos mediante cualquier procedimiento de producción, incluidos los aditivos necesarios para conservar la estabilidad del producto y las impurezas que resulten del procedimiento utilizado, excluidos los disolventes que puedan separarse sin afectar la estabilidad de la sustancia ni modificar su composición.
Preparados: son mezclas o soluciones compuestas por dos o más sustancias.
En una ficha de datos de seguridad debe aparecer información correspondiente a los siguientes apartados:
– Identificación de la sustancia o preparado y del responsable de su comercialización.
– Composición/información sobre los componentes.
– Identificación del los peligros.
– Primeros auxilios.
– Medidas de lucha contra incendios.
– Medidas en caso de vertido accidental.
– Manipulación y almacenamiento.
– Controles de la exposición/protección personal.
– Propiedades físicas-químicas.
– Estabilidad y reactividad.
– Información toxicológica.
– Información ecológica.
– Consideraciones relativas a la eliminación.
– Información relativa al transporte.
– Información reglamentaria.
– Otra información.
Una vez estudiadas las fichas de cada producto que componen un residuo, nos podemos encontrar en tres situaciones:
– Que la sustancia o preparado no sea peligroso.
– Que sea peligroso. Estará identificado con un símbolo de peligro.
– Que no se obtenga información suficiente o concluyente. Se recurrirá a análisis de laboratorio.
Condiciones de envasado y almacenamiento de residuos químicos. Se harán en forma que se evite la generación de calor, explosiones, igniciones, formación de sustancias tóxicas o cualquier efecto que aumente su peligrosidad o dificulte su gestión.
El personal que manipule estos residuos debe cumplir las siguientes normas de seguridad:
– No beber, comer o fumar.
– Utilizar, siempre que sea necesario, equipo de protección personal adecuado: gafas, guantes y/o mascarilla.
– Nunca pipetear con la boca, utilizar medios mecánicos.
– Las superficies de trabajo se descontaminarán periódicamente, siempre que los productos que se utilicen lo hagan necesario y cuando se produzca un derramamiento.
– La operación de vertido en los contenedores de residuos debe hacerse de forma lenta y controlada, interrumpiéndose si se observa algún fenómeno anormal, como la aparición de gas o un aumento excesivo de la temperatura.
– Si la sustancia es muy volátil, se utilizará, para el vertido, una campana de extracción.
– Para el trasvase de líquidos se utilizarán embudos, con objeto de evitar las salpicaduras y los derrames accidentales.
– No utilizar aquellos envases que presenten roturas, deformaciones, no dispongan de tapón o tengan el cierre en mal estado, por la posibilidad de que durante su manipulación puedan presentar fugas o incluso puedan llegar a romperse.
– La boca de los contenedores de los residuos líquidos no debe tener un diámetro grande, para evitar que el contenido del recipiente se desparrame de inmediato en caso de caída.
– Los contenedores no deben llenarse más del 90% de su capacidad, para evitar salpicaduras.
– Una vez terminada la operación de vertido, se cerrará bien el contenedor hasta su próximo uso, con el fin de evitar la exposición de los trabajadores a los agentes químicos.
– Los residuos líquidos se recogerán en garrafas especialmente diseñadas y homologadas para el transporte de mercancías peligrosas por carretera (salvo los citotóxicos). En general estos residuos se recogerán en contenedores amarillos, con una reseña sobre el contenido de los mismos.
3.1.2.3. Grupo IV. Residuos Radiactivos
De la eliminación de los residuos radiactivos se encarga ENRESA (Empresa Nacional de Residuos Radiactivos), que es la empresa que gestiona en España, los materiales contaminados de baja y mediana actividad, de acuerdo con el Real Decreto 1.522/84.
Las instalaciones donde se produce este residuo, para favorecer su gestión, tienen que llevar a cabo una segregación, caracterización y documentación del mismo.
La gestión de estos materiales y sus fuentes, debe llevarse a cabo con arreglo a: principios generales de protección radiológica, normativa vigente y recomendaciones de la Guía de Seguridad del CNS (Consejo de Seguridad Nuclear).
Se puede dividir la gestión de estos productos en cuatro fases:
– Segregación: los productos que son radiactivos de los que no son. De los que son se separarán en razón de su estado físico, naturaleza fisicoquímica y periodo de semidesintegración.
– Caracterización: conocer su actividad y a partir de ella, su actividad específica por unidad de masa.
– Almacenamiento: previo al almacenamiento deberán de etiquetarse con su identificación en la que se incluirá radionucleidos, actividad media estimada en la fecha de cierre, tipo de residuo, instalación de procedencia, tasa de dosis de contacto, fecha de cierre, fecha prevista de evacuación.
– Evacuación: se hará pasado en tiempo para que pueda ser considerado residuo no radiactivo, o cuando llegue la fecha comprometida con la empresa suministradora o gestora de residuos radiactivos.
3.1.2.5. Grupo V. Residuos peligrosos de origen no sanitario
Se podría decir que son productos que teniendo la consideración de peligrosos, son generados en las actividades de mantenimiento y soportes de los Centros Sanitarios. Se incluirían: aceites lubricantes usados, pilas (Ni/Cd, Hg), baterías, filtros bactericidas, tóner de impresoras y fotocopiadoras, envase vacíos de disolventes, aceites, pinturas, barnices y productos de limpieza, etc.
3.1.3. Segregación y envasado.
Dependerá de su clasificación
a) Segregación: se necesitará una adecuada formación de todo el personal involucrado en el proceso de producción del residuo y una adecuada infraestructura para la correcta segregación en el origen sin que se mezclen los distintos grupos de residuos.
Una segregación estricta y normalizada reducirá, en gran medida, la cantidad de ellos que requieran un tratamiento más exigente, manteniendo a la vez los niveles de riesgo al mínimo.
b) Envasado.
– Residuos Envases Contenedores Residuos Generales Asimilables a Urbanos (RGAU) = Bolsa NEGRA
– Residuos Sanitarios Asimilables a Urbanos (RSAU) = Bolsa MARRÓN
– Residuos Sanitarios Infecciosos. Sangre y hemoderivados (>100 ml.) Restos anatómicos (no regulados por D. Policía Sanitaria Mortuoria). Agujas y otro material cortante o punzante (en contenedor punzantes amarillo y luego dentro del verde.) Vacunas vivas y atenuadas. = Contenedor VERDE (Destruible) 60 L. o VERDE (Reutilizable) 60 L. + Bolsa roja – Restos
– Restos de Animales. Residuos considerados Material Especifico de Riesgo Sanitario (MER) = Contenedor AZUL (Destruible) 60 L.
– Residuos Citotóxicos y Citostáticos = Contenedor ROJO (Destruible) 60 L.
– Químicos Sólidos.Reactivos de Laboratorio. Restos pequeños anatómicos conservados en formol. = Contenedor AMARILLO (Destruible) 60 L.
– Disolventes Halogenados (Xilol, Formol…) y no Halogenados.Líquidos de reveladoras.Otros residuos peligrosos líquidos (Líquidos de autoanalizadores…) = Garrafa BLANCA (Destruible) 25 L.
– Mercurio = En bote de cristal o Plástico
– Pilas = Envase Especifico para pilas
– MEDICAMENTOS CADUCADOS (excepto Citotóxicos y Citostáticos) = Contenedor BLANCO (destruibles) 60 L
– Envases Vacíos Voluminosos de residuos peligrosos (con pictograma naranja) de Lavandería, Mantenimiento, laboratorio, Cocina, etc.Filtros campanas flujo laminar. (Con etiqueta de biosanitario peligroso o etiqueta de citotóxico) = Sacos “Big-Bag” 1 m3 Con etiqueta interna indicando el tipo de residuo.
3.2. TRANSPORTE Y ALMACENAMIENTO
a) Gestión intracentro:
– Recogida: la periodicidad va a depender de la zona, la actividad y del residuo que se genera. A excepción de algunos no peligrosos de origen no sanitario, será como mínimo diaria. Cada centro productor establecerá un programa de gestión acorde a sus necesidades.
– Transporte:
• Los envases no se arrastrarán por el suelo, se acercará los carros al lugar de recogida.
• Cuando sean envases perforables, el personal de limpieza cogerá las bolsas por arriba y mantendrá suspendidos y alejados del cuerpo, para evitar posibles pinchazos.
• No se harán trasvases de residuos entre envases.
• El personal de limpieza deberá usar guantes que impidan el contacto directo de la piel con los envases y que protejan de posibles accidentes traumáticos.
• La precaución más importante es que los envases están convenientemente cerrados. Los productores dispondrán de zonas de almacenamiento de los residuos peligrosos para su gestión posterior, bien en la propia instalación, siempre que esté debidamente autorizada, o bien mediante su cesión a una entidad gestora de estos residuos.
– Almacenamiento:
• Temporal. No deberá exceder de12 horas. Este lugar debe estar señalizado, cerca del punto de producción, bien ventilados y con los residuos convenientemente envasados. Sus paredes deben ser de fácil limpieza y no podrán coincidir con circuitos limpios o zonas de tránsito.
• Final. El tiempo de almacenamiento de los residuos peligrosos no podrá exceder de 6 meses. En el caso de los del grupo III A será de 48-72 horas, salvo para aquellos contemplados en los apartados b y e de este grupo. Este plazo no será de aplicación en aquellos centros sin bloque quirúrgico y con una producción de residuos peligrosos inferior a 100 Kg./mes.
b) Gestión extracentro.
Corresponde a la Consejería de Medio Ambiente regular, autorizar y supervisar el correcto cumplimiento de las normas establecidas para la gestión de residuos en el exterior de los centros sanitarios.
– Sistemas de registro y control.
– Todos deben llevar un registro de la producción de residuos en sus instalaciones. Los no peligros se separaran en origen, de aquellos subsidiarios de valoración o reciclado. Tienen que estar en posesión de la documentación que acrediten las entregas realizadas. Los peligrosos se entregarán a gestores autorizados.
– Residuos sanitarios asimilables a urbanos.
– Transporte externo. Se debe realizar igual que con las precauciones de los urbanos. Los Ayuntamientos están obligados a su recogida, transporte y eliminación externa.
3.3. ELIMINACIÓN Y TRATAMIENTO
El tratamiento y eliminación de los residuos sanitarios del grupo III y citostáticos deberá atender a criterios de inocuidad, asepsia y salubridad con el fin de garantizar la eliminación de los gérmenes patógenos y la protección del medio ambiente.
Fuera de los centros, los residuos del grupo II se tratarán y eliminarán como residuos asimilables a los municipales.
Los residuos del grupo III se podrán eliminar mediante incineración, en hornos preparados para esta finalidad y estarán construidos con unas características técnicas definidas.
Se ha de tener en cuenta que cuando se habla de incineración se refiere a incineración efectuada fuera del recinto sanitario y llevada a cabo por empresas autorizadas que ofrezcan toda la garantía de no contaminar el medio ambiente, según la Orden 18 de octubre de 1976 (M. Ind., BB.OO.E. 3-12-1976, rect. 23-2-1977), sobre Prevención y corrección de la contaminación atmosférica de origen industrial, y el Real Decreto- legislativo 1302/86 de 28.6, (M. Obras Púb., B.O.E. 30-6-1986) sobre Evaluación de impacto ambiental.
La generación de residuos biológicos sanitarios representa fundamentalmente un problema de seguridad e higiene en el trabajo, especialmente en el interior de los centros sanitarios, mientras que el riesgo de infección para la comunidad es poco importante y prácticamente limitado a ciertas infecciones no endémicas de España. El riesgo mayor proviene de una incineración inadecuada. Por este motivo, en muchos países, se está imponiendo como medida alternativa a la incineración, el tratamiento de los residuos mediante la esterilización y, una vez triturados, se asimilan a los residuos urbanos.
Otro método de eliminación es el tratamiento por microondas, aunque este es más complejo que el anterior, ya que primero se han de humedecer los residuos pues sólo así las microondas serán efectivas.
Los residuos del grupo III también se podrán eliminar como residuos asimilables a los municipales, siempre que hayan sido previamente tratados mediante esterilización por vapor caliente a presión por técnica de autoclave, es decir mediante acción desinfectante por proceso fraccionado de vapor al vacío.
Los residuos del grupo III que sean cortantes y punzantes, como agujas de bisturí, estiletes y cualquier material metálico que pueda ser vehículo de transmisión de enfermedades, podrán ser tratados mediante esterilización en el mismo centro, y después eliminados como residuos asimilables a los municipales.
La eliminación de residuos citostáticos se realizará mediante neutralización química o incineración a una temperatura que pueda garantizar su destrucción.
Minimización de residuos
Un residuo es un material destinado al abandono y en principio sin utilidad ni valor, por lo que se plantea para su poseedor la necesidad de eliminarlo.
Las técnicas para llevar a cabo esto se dividen en dos grandes grupos:
– Técnicas consistentes en un cambio radical del proceso productivo.
– Las que implican cambios o mejoras en el proceso actual o en sus operaciones relacionadas.
Algunos ejemplos de procesos que persiguen la minimización:
– Potenciar la valoración de los subproductos susceptibles a tal fin: envases de papel, cartón, latas, vidrio, aceites vegetales, etc.
– Buenas prácticas de compras, con el uso de criterios ecológicos: productos en contenedores reutilizables, productos con etiqueta ecológica.
– Buenas prácticas en los procesos: radiografías digitales, reutilización del papel, segregación adecuada en los puntos de producción, etc.
– Buenas prácticas en logística: inclusión en los pliegos de concurso públicos de compras.
3.4. MANIPULACIÓN DE CITOSTÁTICOS
Este apartado está incluido en los contenidos anteriores, pero al ser productos de muy alto riesgo a la hora de su utilización y procesado, se trata de forma independiente.
3.4.1. Vías de entrada
Los medicamentos citostáticos presentes en el ambiente pueden ser incorporados al organismo por:
– Inhalación del polvo o aerosoles, e incluso de los vapores generados a temperatura ambiente.
– Ingestión (comida o cigarrillos contaminados).
– Penetración a través de la piel o mucosas.
– Los cosméticos dificultan la eliminación y pueden dar lugar a exposición continuada.
3.4.2. Factores del riesgo
La magnitud del riesgo depende de:
– La toxicidad inherente de cada citostático.
– Tradicionalmente se han considerado más peligrosos los agentes alquilantes. Los antimetabolitos, por ejemplo, no son mutagénicos en el test de Ames, aunque este hecho no garantiza su inocuidad. En todo caso, éste es un factor sobre el que no se puede actuar ya que viene condicionado por la prescripción médica.
– El nivel de exposición, que se relaciona con:
• La carga de trabajo.
• Las condiciones de manipulación.
– Protección ambiental.
– Material de protección.
– Técnica de manipulación. Implica procedimientos, adiestramiento y evaluación periódica.
• El tiempo de exposición. Es aconsejable aplicar sistemas de rotación entre el personal adiestrado.
• La fase del proceso. Hay mayor riesgo en la preparación y los derrames accidentales, aunque las medidas de protección deben incluir todas las fases del proceso.
• Determinadas características del manipulador. Embarazo, edad reproductiva, exposición simultánea a otros agentes, etc.
3.4.3. Procedimiento de preparación Instalaciones. Área de Trabajo
Características estructurales:
– El área de trabajo estará concebida como un recinto exclusivo con acceso restringido al personal autorizado.
– Constará de al menos dos zonas bien diferenciadas, conectadas entre sí por una zona de paso (en total tres zonas):
– Una antesala destinada al almacenamiento y acondicionamiento del material.
Una zona de paso que sirve de zona transferencia de materiales y personas a la zona de preparación y actúa de barrera frente a la contaminación, tanto microbiológica hacia la zona de preparación, como de productos biopeligrosos hacia el exterior.
En la zona de paso el personal debe colocarse el material de protección cuando vaya a entrar en la zona de preparación y retirárselo cuando circule hacia la antesala. Es aconsejable la instalación de mecanismos que impidan la apertura simultánea de las 2 puertas de la zona de paso.
La zona de preparación propiamente dicha, en que se ubica la CBS. En ella se dispondrán el mínimo número de estantes o armarios, y se almacenará la mínima cantidad posible de material (siempre en muebles cerrados). Se recomienda que las baldas y encimeras no entren en contacto con la pared, dejando libre un espacio de unos 10-30 cm.
Idealmente sólo se almacenará una pequeña cantidad de material cuya finalidad es evitar la salida a la antesala cuando se haya cometido un error en la planificación del material necesario para una preparación concreta.
La antesala y la zona de preparación deben disponer de intercomunicadores de voz, ya que las puertas de comunicación no deben ser abiertas durante el proceso de preparación.
También se aconseja la utilización de materiales de separación que permitan el contacto visual.
– Al menos la zona de paso y la de preparación tendrán la consideración de zonas limpias siendo sus materiales semejantes a los que se utilizan en las áreas quirúrgicas: superficies sin aristas (paredes, suelos, techos, superficies de trabajo), fabricadas con materiales lisos, no porosos y provistos de un revestimiento que permita su lavado con agua abundante (pintura plástica, resina epoxi).
– El aire de ambas zonas debe ser tratado a través de circuitos independientes que controlan tanto la entrada, previa filtración a través de un filtro HEPA, como la extracción. La climatización del aire, que preferentemente se toma del exterior, debe realizarse previamente al filtrado. Los requerimientos en cuanto a calidad del aire no están bien establecidos para instalaciones de este tipo. Muchos autores consideran que los requerimientos de las normativas que regulan la manipulación de productos estériles en el ámbito industrial pueden ser excesivos y probablemente no están pensadas para su aplicación en las unidades de citostáticos hospitalarias.
– El tratamiento de aire permite aplicar gradientes de presión entre zonas para controlar el flujo de aire entre ellas. Dado que en el área de preparación debe aplicarse presión positiva para mantener la asepsia y presión negativa para evitar la salida de contaminantes biopeligrosos hacia zonas adyacentes, existe cierta controversia sobre cuál de los 2 aspectos debe prevalecer. En nuestra opinión la zona de preparación debe someterse a presión negativa para minimizar el riesgo de contaminación del entorno. Paralelamente, la zona de paso debe tratarse con presión positiva, de manera que el aire que ingrese a la zona de preparación, al proceder de esta zona que también recibe aire filtrado, sea de calidad suficiente – Las CBS clase III (aisladores) pueden ser instaladas en zonas con menos requerimientos de calidad de aire y presiones diferenciales ya que se trata de sistemas más herméticos.
Zonas del área de preparación con las presiones diferenciales.
Normas en el área de trabajo
– No se permitirá comer, beber, masticar chicle, fumar ni almacenar alimentos.
– Se evitarán las corrientes de aire y los movimientos bruscos que puedan provocar turbulencias en el flujo laminar de la CBS.
– El personal no utilizará maquillaje ni otros productos cosméticos ya que pueden provocar una exposición prolongada en caso de contaminación.
Asimismo durante el trabajo debe evitarse el contacto de los guantes con áreas susceptibles de ser contaminadas y en particular el contacto con la cara.
– El paso a la zona de preparación se restringirá al máximo, siendo obligatoria la colocación de todo el material de protección.
La limpieza de la sala tiene una doble finalidad:
– Mantener las superficies limpias de polvo para mantener la clase de la sala y minimizar la carga bacteriana.
– Descontaminación de trazas de citostáticos.
El suelo se limpiará diariamente con una mopa por arrastre (nunca se barrerá) y a continuación con un detergente desinfectante (como los usados en quirófano) o con lejía. La limpieza de las paredes se hará semanalmente con agua y jabón. El material de limpieza se considerará exclusivo para el área de preparación y se desechará como si estuviera contaminado.
El personal que lleva a cabo la limpieza de la sala de preparación estará debidamente entrenado e irá provisto de material de protección.
Cabina de Seguridad Biológica (CBS)
Las preparaciones de citostáticos deben realizarse en Cabinas de Seguridad Biológica (CBS).
Clase II tipo B o Clase III (Aislador), de flujo laminar vertical.
Deberán estar certificadas y cumplir los estándares internacionales.
Asimismo es importante cuidar del mantenimiento de las mismas que se realizará por personal cualificado, quedando siempre debidamente documentadas.
Esquema de funcionamiento de una CBS.
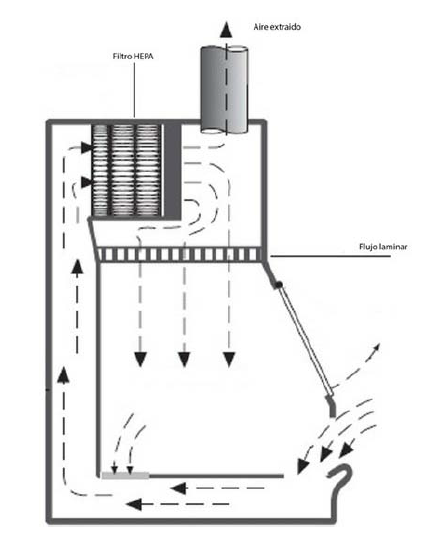
Clasificación
– Clase I: No recomendada para el manejo de citostáticos. Proporciona protección para el manipulador y el ambiente pero no para el producto. Constan de un solo filtro HEPA en la salida del aire al exterior.
– Clase II: El funcionamiento, el flujo de aire vertical tras atravesar un filtro HEPA alcanza la superficie de trabajo, se bifurca a través de las rejillas de la misma y continua circulando por un septo interior hasta que, tras un nuevo filtrado, es impulsado por una bomba en parte de nuevo a la superficie de trabajo y el resto a través de una nueva filtración al exterior de la cabina. Se crea así una presión negativa que se compensa con la entrada de aire exterior por el frontal de la cabina. Es precisamente esta cortina de aire exterior la que actúa como protección para el manipulador.
La protección del producto vendrá definida por la proporción de aire exterior absorbida y la calidad del mismo.
– Clase III (Aisladores) Son compartimentos de trabajo totalmente cerrados de forma que la zona de trabajo queda totalmente aislada. El aire se introduce a través de un filtro HEPA y la salida es mediante doble filtración. La manipulación se realiza a través de unos guantes fijos incorporados en la misma cabina.
Los materiales se introducen en ella a través de una cámara de transferencia. Para manejo de citostáticos se recomienda que trabajen a presión negativa. En principio los requerimientos de área limpia son menores que con las de clase II.
Entre sus inconvenientes cabe destacar una mayor dificultad de operatividad que exige un período de entrenamiento mayor por parte del personal.
Con ellas se consigue protección tanto para el manipulador como para el producto.
Procedimiento de tratamiento de residuos
Se consideran residuos citostáticos:
– Los restos de medicamentos Citostáticos generados en la preparación y administración.
– El material utilizado en la preparación y administración (agujas, jeringas, frascos, bolsas, sistemas de infusión…).
– El material de protección de los manipuladores (ropa protectora desechable, guantes, mascarilla…).
– El material utilizado en la limpieza de las zonas donde se lleva a cabo la manipulación (especialmente la preparación y administración).
– El material procedente del tratamiento de derrames accidentales.
Material necesario
– Contenedores rígidos específicos para el material cortante y/o punzante que una vez llenos se depositarán en:
– Contenedores de mayor volumen preferiblemente rígidos (algunas comunidades admiten contenedores semi-rígidos o bolsas de plástico de galga superior a 200), de material que no emita gases tóxicos en su incineración, con cierre hermético. Estarán identificados con el rótulo que corresponda en función de la Comunidad Autónoma que corresponda.
Manipulación y almacenamiento
– Los contenedores nunca se situarán en lugares de paso dentro de las unidades donde se manipulan citostáticos y se retirarán cada 12-24 horas.
– El almacenamiento final se hará de forma independiente del resto de residuos, en lugar ventilado y a ser posible refrigerado. El tiempo máximo permitido varía en función de las legislaciones autonómicas y está en función de la temperatura pero a temperatura ambiente nunca será superior a 72 horas.
– Durante todo el proceso de recogida y traslado de las bolsas y contenedores, es necesario que se asegure el mínimo contacto del personal con el contenido de estos recipientes. Por ello deberá contar con los medios de protección adecuados para evitar riesgos derivados de la manipulación de estos residuos.
Eliminación
– La eliminación de estos residuos se realizará mediante la recogida de los mismos por una empresa autorizada para ello y su posterior incineración.
– La incineración debe realizarse a 1.000 ºC en hornos provistos de filtros que protejan el medio ambiente es el sistema más idóneo para la eliminación de citostáticos.
– Se desaconseja la inactivación química al ser un proceso complejo que implica multitud de procedimientos distintos en función del material de que se trate.
3.4.4. Tratamiento de las excretas de pacientes con tratamiento citóstatico
Se debe tener presente que una fracción variable de los fármacos se eliminan del organismo humano sin alteración, y que en muchas ocasiones sus metabolitos poseen actividad citotóxica, pudiendo ser esto especialmente importante cuando se administran dosis altas de estos medicamentos. El tiempo de eliminación de un fármaco es variable en función de su farmacocinética, dosis aplicada y vía de administración. A continuación se documenta los tiempos de eliminación de distintos fármacos citostáticos.
Las excretas deberían de recibir el mismo proceso de eliminación que el resto de residuos citostáticos, pero razones de factibilidad hacen que actualmente sea muy complejo cumplir con lo recomendado. Como mínimo, debe disponerse de baños dotados de un sistema que permita el lavado continuo o bien disponer de un sistema de evacuación independiente y dirigido a un colector para materiales peligrosos hospitalarios, con arqueta de registro. Sin embargo, deben dictarse unas normas para que el personal sanitario tome medidas de protección, como en el caso general de la manipulación de citostáticos, llevando dobles guantes de látex, bata impermeable, mascarilla y gafas de protección cuando exista riesgo de salpicadura, y evitando todo contacto cuando se estén manipulando estas excretas. Si no es posible tratar las excretas con un neutralizante específico, serán abocados al desagüe diluidos con una gran cantidad de agua.
Cuando se utilicen las excretas para la determinación de pruebas analíticas, la recogida, almacenamiento y manipulación deberá realizarse con especial precaución.y que esté muy contaminada con excretas y vómitos se desecharán en las bolsas destinadas a los contenedores de residuos citostáticos. Si esta lencería estuviera poco contaminada se colocará en unas bolsas de material lavable y éstas, a su vez, en unas bolsas impermeables identificadas. Una vez en la lavandería, tras retirar la bolsa impermeable, se sumergirán en lejía y posteriormente se procederá al lavado habitual. El personal directamente en contacto con la lencería deberá ir protegido con guantes de látex y bata.
3.4.5. Protocolo de derrames de productos citotóxicos
Kit de derrames de citotóxicos
– Cantidades suficientes de papel absorbente (o polvo), gasas o toallas absorbentes, mejor si están impregnados de sustancias absorbentes como alginatos.
– Dos pares de guantes de polivilino o neopreno.
– Calzas para zapatos, gafas protectoras y bata.
– Mascarillas protectoras desechables para polvo, vapores y aerosoles.
– Dos bolsas de residuos citostáticos claramente etiquetadas.
– Cantidad apropiada de solución alcalina o lejía.
– Botellas de agua para eventuales irrigaciones.
– Recogedor y escobillas desechables.
– Todo el personal que maneja sustituir por manipula fármacos citostáticos debe familiarizarse con los procedimientos a seguir en caso de derrames.
Procedimiento a seguir en caso de derrames
En caso de derrame de material citostático en cualquier área que no sea el interior de una cabina citotóxicos el procedimiento es el siguiente:
– Sacar el contenido del kit y colocarse la mascarilla, bata desechable de baja permeabilidad, gafas de seguridad, gorro, calzas y dos pares de guantes.
– Limitar el área del derrame: colocar gasas o paños, mejor si están impregnados de sustancias absorbentes (alginatos), para cubrir el líquido del derrame y dejar que se empape. Si hubiese polvo en el derrame estas medidas se extremarán ya que el peligro de aerosoles es mucho mayor, para minimizarlo se colocará una gasa o paño y sustituir por procederemos a mojar mojamos con precaución esta gasa para que el polvo se disuelva y se absorba.
– Con ayuda de gasas, introducir los residuos en bolsas de plástico, de color rojo y de galga 400, cerrarlas con grapas y echarlas al contenedor.
– Limpiar el suelo contaminado, utilizando la fregona y el cubo reservado para este uso, en primer lugar con agua jabonosa. Después verter lejía concentrada en la zona contaminada y fregar posteriormente con solución de lejía diluida.
– Desechar el material empleado en la bolsa de residuos citostáticos.
– Todo el material contaminado deberá disponerse en unas bolsas de plástico resistentes, de galga 400, la cual permita el almacenamiento seguro de estos residuos e impida su rotura (sobre todo por objetos punzantes como agujas o trozos de vidrio). Las bolsas deben de estar rotuladas de forma que adviertan que el material que contienen está contaminado con citostáticos. Dichas bolsas se almacenarán en un contenedor rígido desechable hasta proceder a su eliminación final.
– En el caso del uso de contenedores de un solo uso no se hace necesario el envasado previo en bolsas.
– En ocasiones si el derrame es de gran dimensión podrían utilizarse sustancias neutralizantes. Pero esta práctica no está exenta de riesgo por tratarse de productos químicos irritantes, cuyo manejo inadecuado, o eventual rotura del envase que lo contiene, podría dar lugar a lesiones en los manipuladores. Para que la neutralización sea efectiva es necesario un tiempo idóneo de contacto que excede el tiempo prudencial de solución de un problema por derrame. Otro inconveniente es que existen lagunas de conocimiento sobre la toxicidad de los productos resultantes de la neutralización. Además, los agentes neutralizantes tienen caducidad y periódicamente habría que reponerlos con una nueva fabricación lo que aumentaría la probabilidad de accidente en los técnicos preparadores ya que son sustancias irritantes y corrosivas.
– Por todo ello no parece aconsejable distribuir pequeñas muestras de agentes neutralizantes en el kit de derrame que se localizan en las unidades clínicas donde se realizan la administración de los medicamentos citostáticos. Si debe figurar en el protocolo de derrame la consigna de que ante la ruptura o derrame de un preparado citostático, debe llamarse lo antes posible al Servicio de Farmacia, que evaluará la conveniencia o no de un tratamiento con agentes neutralizantes.


